(2017年3月3日更新) [ 日本語 | English ]
HOME > Plant list (植物リスト) > ツユクサ科 (Commelinaceae) > ムラサキツユクサ
ムラサキツユクサ (Tradescantia L.)ムラサキツユクサ (紫露草)生活型: 多年生草本 |
分布: 新大陸 (日本では帰化種) 生息地: 日本では都市部に多い |
 1
1
 2
2
 3
3
 4
4
[1] 1988年6月18日、札幌市桑園道路沿。[2-4] 2008年8月30日、札幌市東区の未舗装駐車場
| 気孔観察 (observation of stoma) | |
|---|---|
|
ムラサキツユクサ葉裏の表皮をピンセットで取りプレパラート作成 倍率15 × 20が普通最適 絞りは最も絞った段階で観察 15 × 20では、気孔・細胞壁・細胞膜・核程度は確認可能 より高倍率でも、その他オルガネラ観察は困難 15 × 20でも副細胞では殆どオルガネラが見えない Cf. Azolla japonica Franchet Sav (オオアカウキクサ, サンショウモ科) |
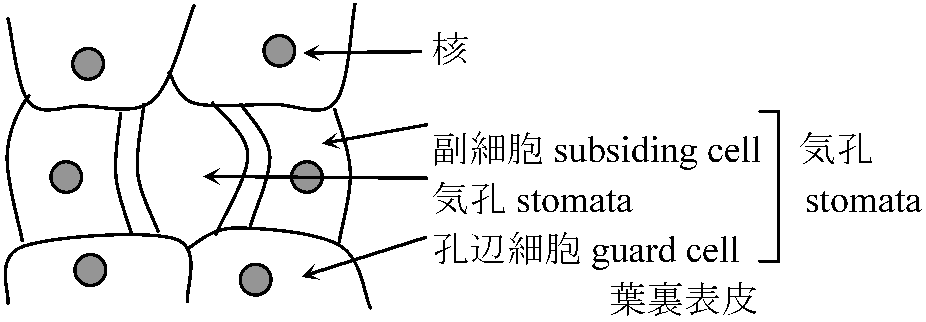
|
| 花粉発芽 (observation of pollen germination) | |
|
花粉は普通(自然界では)柱頭上で発芽 人為的誘導可能: 柱頭抽出液、0.3-0.7 M蔗糖液、蔗糖寒天培地等の人工培地上(pH 6.0-6.8)で、適当な湿室中で花粉は発芽し花粉管を伸長させる 花粉発芽プロセス
野外: 花粉発芽能力は早朝から数時間しか保持出来ない 準備人工培地調製
実験1発芽前形態観察 スライドグラスに花粉をまき、酢酸カーミン一滴加え固定染色 |
カバーグラスを掛け検鏡 スケッチ ポイント: 生殖核と花粉管核の違い。前者の周りには濃染される細胞質がとりまいている 実験2花粉管伸長(培地が冷えるのを待って)
記録例: 時間(分) _____ 測定値(長さ) _____ 注) 乾燥を防ぐため観察測定は迅速に行う。実験3発芽後の形態観察花粉管伸長が大体プラトーに達した頃、寒天ごと観察した花粉を含む部分を剥ぎとり、スライドグラスに載せる 酢酸カーミンを一滴加えカバーグラスをかける ガスバーナーでわずかに熱をかけ寒天を溶かす → 検鏡 (観察) 花粉管の先端部と核に注目してスケッチ ポイント: カロース栓、2ケの精核、花粉管核 |
|
ムラサキオモト (紫万年青) シキンラン (紫金蘭) 生活型: 常緑多年草 原産地: 西インド諸島 - メキシコ 利用: 園芸 (教材) |
🍹葉(根際で切取り長さ3 cm程度に刻みガーゼに詰める)
熟成1ヶ月 - 中身引抜く |
 1
1
 2
2
 3
3
[1-3] 2017年1月24日、北海道大学生物実験センター温室
| 原形質分離 (plasmolysis) | |
|---|---|
|
顕微鏡観察 → 細胞浸透価判定 材料: ムラサキオモト 準備: 蔗糖 saccharose (分子量 342.30)、各種ガラス器具 方法
|
原形質分離細胞比率 75-100% 30-75% 10-30% 10% |