(2025年11月4日更新) [ 日本語 | English ]
HOME > 講義・実習・演習一覧 / 研究概要 > 小辞典 > 代謝
代謝 metabolism生体内に取り込んだ分子の酵素等による変化 = 物質代謝 + エネルギー代謝生物が栄養物からエネルギーを得て、エネルギーを細胞物質に使用する時に必要とする一連の化学反応 主機能:
ATP 有機物質 ATP 生命活動: 生合成、運動(アメーバ、鞭毛、繊毛、筋肉)、体温(発熱)、能動輸送(Naポンプ)、発光 Ex. ウミボタル、発電 Ex. シビレエイ エネルギー代謝 energy metabolism生命現象に伴う(原因となる)エネルギー出入input/outputや変換translation特徴: 化学結合エネルギー(呼吸発酵)や光エネルギー(光合成)が直接熱転化される前にATP等の高エネルギー結合に捕らえられる
転化効率30-60%で、熱転化部分は体温保持や蒸散による冷却補償に充てられる 物質代謝 substance metabolism同化作用 anabolism: 原料物質の化学的複雑性を増加させる化学変化。通常、吸エルゴン的過程で、平行して進行する発エルゴン反応(異化作用)から吸収される自由エネルギーにより反応進む
独立栄養生物は外部からこのエネルギーを吸収
炭酸同化 窒素同化 取入れる養分形 |
Q. 次のa-dの4組の述語をanabolismまたはcatabolismに通常関係づけられている様に分類せよ a) 合成、分解 b) ADPとPiからのATP生成と連関、ATP分解と連関 c) エネルギー消費、エネルギー合成 d) NADからNADHの生成と関連、NADHからNAD生成と関連
エネルギー源
生物エネルギー論 bioenergetics (最近あまり聞かない言葉だが)
光
光栄養
+ H2O: 酸素発生型光合成
生物のエネルギー獲得・変換・利用を研究 - 細分化で死語化? |
生体が構成成分(生体分子)を作ること
生合成研究
基本技術: 生成物阻害product inhibition – allosteric, homosteric 基本ポリマーの生合成
ΔG0' < 0, ΔF |
代謝における正常生合成経路= 無傷な系intact / 成熟した系mature / 老衰していないnot senecent (正常な系は1つとは限らない)
株 成長有
成長無 (b) (a)でなされた構成が成立するには大きな仮定が3つある。これを説明せよ Q. ある細菌の生合成系の調節は図のようになっている
┌────────────────┐
♦ ♦↗ E → F A ⇉ B → C → D ♦ ♦↘ G → H └────────────────┘ 図. 化合物A-H、各段階の反応、ま たはそれを触媒する酵素を1-7、 ♦はフィードバク阻害を示す。 a) 今過剰のHをこの細菌に与えた時にA-Hの反応のどれが減少するか。ただし反応|hは正常量のHを合成するのに必要なだけのBを合成する b) 大過剰のDをこの細菌に与えた時に起るA-Hの変化を全て述べよ c) 今酵素 |f を欠く変異株が存在する時、これに過剰のFを与えた時のA-Hの変化を全て述べよ |
呼吸とエネルギー代謝 respiration and energy metabolism自家呼吸: 高等植物は細胞内に糖質、脂肪等養分を多量に貯え呼吸材料を与えなくても呼吸は長く持続可能⇔ 細菌等貯蔵養分の少ない生物は、自家呼吸は比較的短時間で衰退し種々物質を与えると、これを材料に酸化を行い呼吸回復する。呼吸材料は糖が最もよく使用される 生体における酸化還元反応呼吸系に置ける酸化還元:
C6H12O6 + 6O2 = 6H2O + 6CO2 + ATP ATP = energy, 普通は38ATP, 688 kcal
エネルギー効率C6H12O6 → 6CO2 + 6H2O______ ΔG0 ≈ -686 kcal (-2872 kJ)C6H12O6 → 2C2H5OH + 2CO2___ΔG0 ≈ -54 kcal (-226 kJ) ΔG0: ギッブスの自由エネルギー変化量
A + B ⇔ C + D … ΔG0: (1 mol変化時の)標準条件下自由エネルギー変化量) ΔG = ΔH - TΔS ΔH = エンタルピー変化量 = [A, Bの内部エネルギー] - [C, Dの内部エネルギー]
T = 絶対温度
ΔH = ΔE + PV … ΔE = 総エネルギーの変化量
__K'eq_____ΔG0_____Reaction
ΔG0 < 0: 反応は自発的spontaneousに進行 = Exergonic、エネルギー放出反応
K'eq__________0.001__ 0.01___0.1__1.0___10__ 100__ 1000 高エネルギー結合体 high-energy compounds加水分解時の遊離エネルギーの大きいもの
ATP
~: 高エネルギーリン酸結合 ATP + H2O → ADP + Pi 反応早く平衡見分けにくい Condition: ph 7.0, 37°C, excess Mg++, Hexokinase |
ATP + glucose H.K. → ADP + Glu-6-P
K'eq = 66.1, ΔG10' = -4 kcal (-17 kJ) Glu-6-P + H2O phosphate → Glucose + Pi K'eq = 171, ΔG20' = -3.3 kcal (-13.8 kJ) ΔG0' = ΔG10' + ΔG20' = -7.3 kcal/mol (-30.6 kJ/mol) 高エネルギーリン酸化合物 (high-energy phosphate compound)ATPの生体内での働きATPは生体内で多様な働きをしているエネルギー獲得反応(還元反応)
供給体 electron donor: 還元剤 donor ⇔ acceptor + e- 酸化還元電位 (oxidation-reduction potential, or redux potential → 起電力 → ATP形成
A + 2e- + 2H+ → AH2 呼吸 respiration: 異化の一種基本式有機呼吸aerobic respiration
AH2 + 1/2O2 → A + H2O
AH2 + NO3- → A + NO2- + H2O
Glucose → Luctose 呼吸単位・呼吸速度呼吸率 respiratory quotient, QO2μl O2/g weight/hour(min)等の単位重量・単位時間あたりμl O2吸収量(呼吸の強さ)- CO2の出入を考慮していず呼吸を表現するのは不十分 QCO2: μl CO2/g weight/hour(min) etc. - 単位重量・単位時間あたりに何μlのCO2を排出するかを表す
ニンジン_____________根___成熟葉__ 若葉 炭水化物(glucose): RQ = 6CO2/6O2 = 1 ∵ C6H12O6 + 6O2 → 6CO2 + 6H2O タンパク質 RQ ≈ 0.8脂質 (glycerol triolate): RQ = 57/83 = 0.69 ∵ C57H104O6 + 83O2 → 57CO2 + 52H2O アミノ酸 (citrate): RQ = 6/4.5 = 1.33∵ C6H8O7 + 4·1/2O2 → 6CO2 + 4H2O ⇒ 呼吸基質の割合推定可 = 呼吸基質に何が使われているかを推定可馬: RQ = 0.96 (草食) > ヒト: 0.89 (雑食) > 犬: 0.79 (肉食) Ex. 酒: C2H5OH + 3O2 → 2CO2 + 3H2O ∴ RQ = 2/3酒が全て体内燃焼 - RQは2/3に近づく (実際には体温維持に使われる) 測定方法: 原理 = 排出CO2量か吸収O2量を計る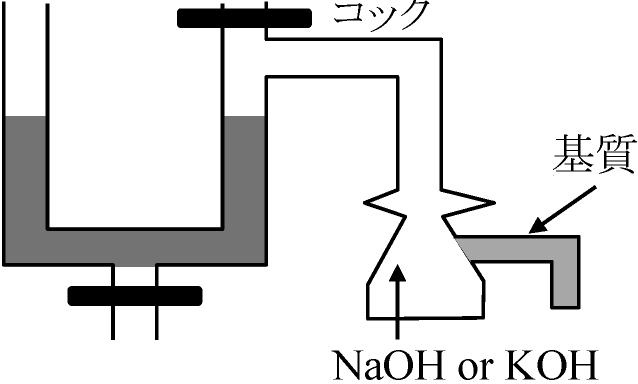 1. 検圧法manometric method
1. 検圧法manometric method
反応 → アルカリ O2 uptake, CO2 evolve
- Pt________2O2 + 2H2 + 4e- → 4OH- CO2: 赤外線(IR)を強く吸収 - IR吸収量測定でCO2量変化(= 吸光量)推定 → 光合成量測定でも利用 |
|
1791 Lavoisier: 静脈・動脈色違う ⇒ ヘモグロビンhemoglovin構造の違い 1840 Schoenbein: オゾン(O3)発見 ⇒ 生体内酵素活性化説 activated oxygen theory → 生体内O3発見されず否定 1884 MacMunn Keilin (1925)が実験結果を当時の技術で示し色素存在指摘。筋肉中ミオグロビンと異なる色素存在に着目し、その異なる色素は鉄を含む物質と考えたが、発見できず実際若干異なる物質であったためミオヘマチンmiohematinと呼ばれる。類似現象は酵母でも発見され、これが呼吸に関連することも予測された。酵母にCN-を加えると呼吸阻害されるが酸化されないため吸収バンドは残り観察できる 1850 Garreau, Lazare1885 Ehlich: 水素活性化説 activated hydrogen theory 1903 Wieland: 理論上の酸化(実際の酸化では脱水素が多い)
-CH=O → -C(OH)=O |
1908 Warburug, O.: ウニ未受精卵
Feを添加すると呼吸促進 → CN, COを入れると阻害 A: 呼吸基質, Fe: atmungs ferment
Mbは還元(脱水素)が無酸素ステージでも可能
a b c β バンド 生物をホモジェナイズすると酸化還元状態の違いで吸収帯に差出る → 還元状態(Ex. ラクトースを多量に加える)に放置すると吸収帯消失 |
|
= 解糖系 + TCA回路 + 電子伝達系 = クレブス回路とそれに関与する代謝経路 呼吸は、解糖系を除くと、特にTCA回路はミトコンドリア中で多くの酵素が関与し行われる。生体酸化還元において電子伝達に関与する一連の酸化還元酵素系のことで、通常ミトコンドリア等の分子状酸素によるNADHおよびコハク酸などの酸化酵素系を指す
呼吸鎖の大きな流れは: 解糖系 → TCA回路 → 電子伝達系
A → B
AH2 + 1/2O2 → A + H2O
発酵: 嫌気的生物 呼吸鎖研究多くの経路がアンチマイシンA (antimycin A)、ロテノンrotenone、アミタールamytal、ピエリシジンpiericidin等の阻害剤を利用し確認された解糖系 glycolysis (= EMP経路)細胞質基質内で行われる、炭素化合物(糖質)からエネルギーを引出す形式 [開始] グルコースのリン酸化 → … →[終了] ピルビン酸の乳酸への還元
外界と酸化還元当量のやりとりをしない嫌気的エネルギー獲得形式
Glucose + ATP → Glucose 6-phosphate + ADP
G-6-P → Fructose-6-phosphate
F-6-P → Fructose 1,6-biphosphate (ΔG0' = -3.4 kcal) F-1,6-P2 → Dihydroroxyacetone phosphate (DHAP) + Glyceroaldehyde 3-phosphate (Ga3-P) (ΔG0' = +5.73 kcal) (5) Triosephosphate isomerase (EC 5.3.1.1)DHAP → Ga3-P 可逆反応 (6) Glyceroaldehyde 3-phosphate dehydrogenase (EC 1.2.1.12)
RCHO + NAD+ + H2O → RCOOH + NADH + H+ (ΔG0' = -10.3 kcal) [10.3 - 11.8 = -1.5 kcal]
1,3-diphosphoglycerate - H3AsO4 (解糖の脱共役剤 uncoupler) 1,3-DGP + ADP ⇔ 3-P-G + ATP (8) Phosphoglycerate mutase (EC 5.4.2.1)3-P-G ⇔ 2-P-G (9) Enolase (EC 4.2.1.11)
2-P-G ⇔ Phosphoenol pyruvate (PEP) + H2O, PEP: 高エネルギーリン酸化合物
PEP + ADP → Pyruvate + ATP____ΔG0' = -7.5 kcal Pry + CO2 +ATP + H2O → Oxaloacetate + ADP + Pi ② Malate dehydrogenase: OAA + NADH + H+ → Malate + NAD+ 反応ミトコンドリア内で起り、オキザロ酢酸は膜を通れないがリンゴ酸は運搬体の働きで膜を通過しサイトプラズムに出られる ③ Malate DH (cytplasm): Malate + NAD+ → OAA + NADH + H+ ④ Phosphoenolpyruvate carboxykinase:
有機酸(OAA, Malate, etc.)と糖合成反応の接点となる酵素
Pyr → Acetoaldehyde + CO2
Pyr + NADH + H+ &hAarr; Lactate + NAD+ Acetoaldehyde + NADH + H+ ⇔ Ethanol + NAD+ 解糖系酵素の特徴EC 酵素数 1 Oxidoreductases 2 ┌加水分解酵素・合成酵素がない 2 Transferases 4 │加水分解酵素無 → エネルギーロス少 3 Hydrolases 0 ┤酸化還元酵素はATP合成でしか使わない 4 Lyases 2or3 │→ TCA回路と異なる点 5 Isomearses 3 │分子変形が多い 6 Ligases 0 ┘ 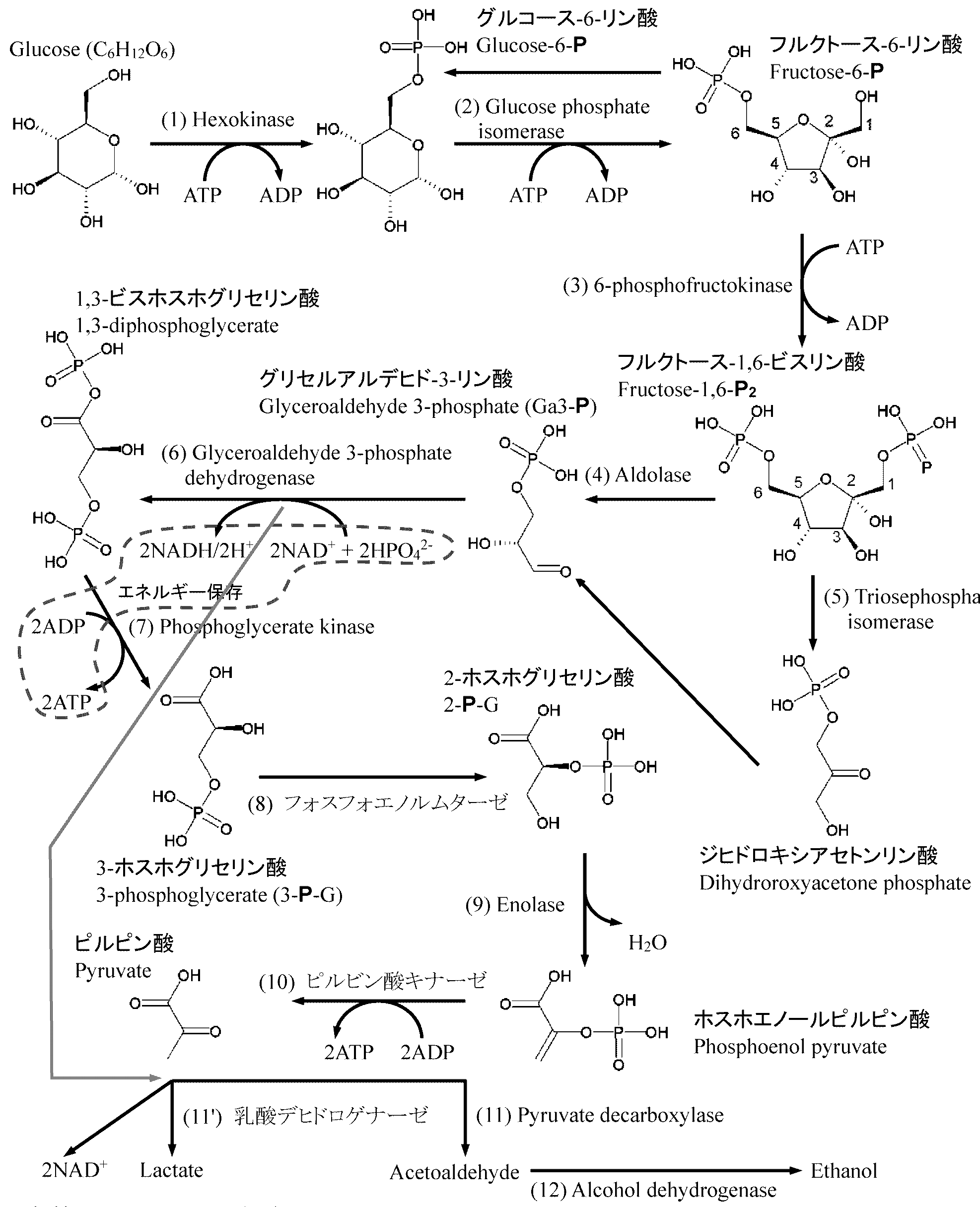 図. 解糖系 glycolysis (EMP経路) ホスホグルコン酸回路 (phosphogluconate pathway)別名 Pentose phosphate pathway1958 Wakil: 以下を実験的に証明 malnyl-CoAが脂肪酸合成の本体でacetyl-CoAはその阻害剤 1960 Mosbach1961 Bentley: malonyl-CoA → orsellinate → penicillate 1961 Lyneu 1961 Bu'Loch: -OOC-C*H2-COO- ⇒ 1978までに脂肪酸合成経路は解明される 代謝経路の酵素はサイトプラズム(ミトコンドリア細胞質の溶性部分)にある。脂肪酸合成が盛んなところ(肝臓・乳腺等)ではNADPが必要なのでこの経路の代謝が盛んに起こる 機能
G6P (アルデヒド) + NADP → NADPH + 6-P-gluconate (カルボン酸) (2) 6-P-gluconate dehydrogenase_________EC 1.1.1.43(3) Ribose-5-phosphate isomerase________EC 5.3.1.6 (4) Ribulose-5-phosphate 3 epimerase_____EC 5.1.3.1 - 異性体作る (5) Transketolase______________________EC 2.2.1.1 Pentose + Pentose → Hepsose + Triose (6) Transldolase_______________________EC 2.2.1.2Heptose (3/7) + Triose → Hexose + Keto- (7) Heptose (4/7) + Pentose (2/5) → Hexose結果としてNADPの供給が行われる
EC 1 2 3 4 5 6
酵素数 2 2 0 0 2 0
Acetyl-CoA + CO2 + ATP → Malonyl-CoA + ADP + Pi7malonyl-CoA + Acetyl-CoA + 14NADPH + 14H+ → Palumitate + 7CO2 + 14NADP+ + 8CoA-SH + 6H2O 解糖の逆反応による糖合成光合成を行わない生物の糖合成glyconeogenesisは3つを除き解糖の逆反応Glycogen (α-1,4-glucoside linkage)
代謝産物(lactose, ethanolなど)が還元されNADHが酸化されNAD+へ入る 好気的状態 Glucose →→→ Pyruvate → C2O, H2O__呼吸
酸素を還元して NADH → NAD+: TCA回路 TCA回路= トリカルボンサン回路・クエン酸回路・クレブス回路, tri-carboxyl cycle1937 Krebs HA: TCA回路決定 解糖及びその他異化作用により生じたAcetyl-CoAを完全に水とCO2に分解する好気的過程 → 呼吸鎖 解糖系導入物質がglucoseであればこの回路は3回転しglucose 1分子が完全酸化される この時の水素はNAD+等へ回されNADHの酸化還元電位差によって生じる酸化的リン酸化に使用される 糖・アミノ酸・脂肪酸完全分解と最大エネルギー引出しが可能。呼吸鎖と共役しAcetyl-CoAがこの回路で完全酸化を受ける(ΔG0' = -272 kcal)と12分子ATPが生じる(ΔG0' = +110 kcal) → エネルギー回収率 ≈ 40% ⇒ ① NADHの供給、② アミノ酸合成の中間体の供給といった両面的性質amphibolic natureがある TCA回路の他の生理的役割は生体構成脂質合成への原料供給。TCA回路回転の強さはその含まれる物質量に依存するので合成諸回路へ物質引上げを補給する必要があり、ピルビン酸カルボキシラーゼあるいはグリオキシル酸回路等が関与している。クエン酸回路はミトコンドリア内溶性部分(マトリックス)に局在する 補充反応 anaplerotic reactionTCA回路の中間体欠乏を補充する反応Ex. アミノ酸からアミノ酸を作る反応を言う。※すべてCO2固定反応 (1) Pyruvate carboxylase (ピルビン酸カルボキシラーゼ)
Pyruvate + CO2 + ATP → OAA(リンゴ酸) + ADP + Pi(ATP消費) Pyruvate + NADPH + H+ → OAA + NADP+ (3) Phosphoenol pyruvate carboxykinase (PEP)PEP + CO2 + GDP → OAA + GTP 酵素系1. Pyruvate dehydrogenase EC 1.2.4.1
Pyruvate + Co-A-SH + NAD+ → Acetyl-CoA + NADH + H+ +CO2 b) E1-TPP-CHOH-CH3 + E2 ________________________ S___S_________CH3-SO___ SH c) E2 ______S___ SH__________ S___ SH ______ | ___ O=C-CH3 d) E2 ______S___ SH_____________S───S__Lipoamide dehydrogenase e) E3-FADH + NAD+ → E3-FAD + NADH + H+ 2. Citrate synthase EC 4.1.3.7 Acetyl CoA + DAA → Citrate + CoA-SH: ATP, NADHで阻害 3. Aconitae EC 4.2.1.3Citrate(91%) ⇔ cis-Aconitate (3%) ⇔ iso Citrate (6%) ← 平衡状態  4. Isocitrate dehydrogenase:
4. Isocitrate dehydrogenase:NAD要求性 EC1.1.1.41 NADP要求性 EC1.1.1.42
iso Citrate + NAD+ (or NADP+) → α-ketoglutarate + CO2 α-ketoglutarate + CoA-SH + NAD+ → Succinyl-CoA + NADH + H+ + CO2
Succinyl-CoA(1 mol) + GDP → Succinate + GTP
ミトコンドリア膜に硬く結合した酵素複合体。補酵素はFAD Fumarate → Malate 8. Marate dehydrogenase EC 1.1.1.37Malate + NAD → OAA + NADH + H+ 酵素命名規約に基づいて整理: EC/酵素数 = 1/5* 2/0 3/0 4/2 5/0 6/0
⇒ TCA回路は酸化還元酵素が反応の主役 COOH-CO-CH2-CH2-COOH (OAA) + NH3+ + NADH + H+ __→ COOH-CHNH2-CH2-CH2-COOH (Glutamate)
OAA_____ → glutamate アミノ酸中間体intermediatesになっている ミトコンドリア中に貯まったOAA(オキザロ酢酸)は
OAA + glucose → [transaminase] → aspatrate + α-KG → 2Pyr + 2ATP + 2NADH + 2H+ + 2H2O: 可溶部分での反応 TCA cycle: 2NADH + 2H+ + O2 + 6Pi + 6ADP→ 6ATP + 2NAD+ + 8H2O: ミトコンドリア内の反応
↓ Total 8ATP: 解糖でできたNADHを酸化
ATP products
1. PyrDH -NADH + H+ 3 2. I,C,DH –NADH 3 3. α-KGDH –NADH 3 + 1(+1は基質レベル) 4. Succ-DH –FADH2 2 5. MDH –NADH 3 Total 15ATP × 2 → 8ATP + 15ATP × 2 = 38ATP 基質がグリコーゲンだと39ATPになる エネルギー効率 (7.3 × 38)/685 (kcal) × 100 = 41.5% 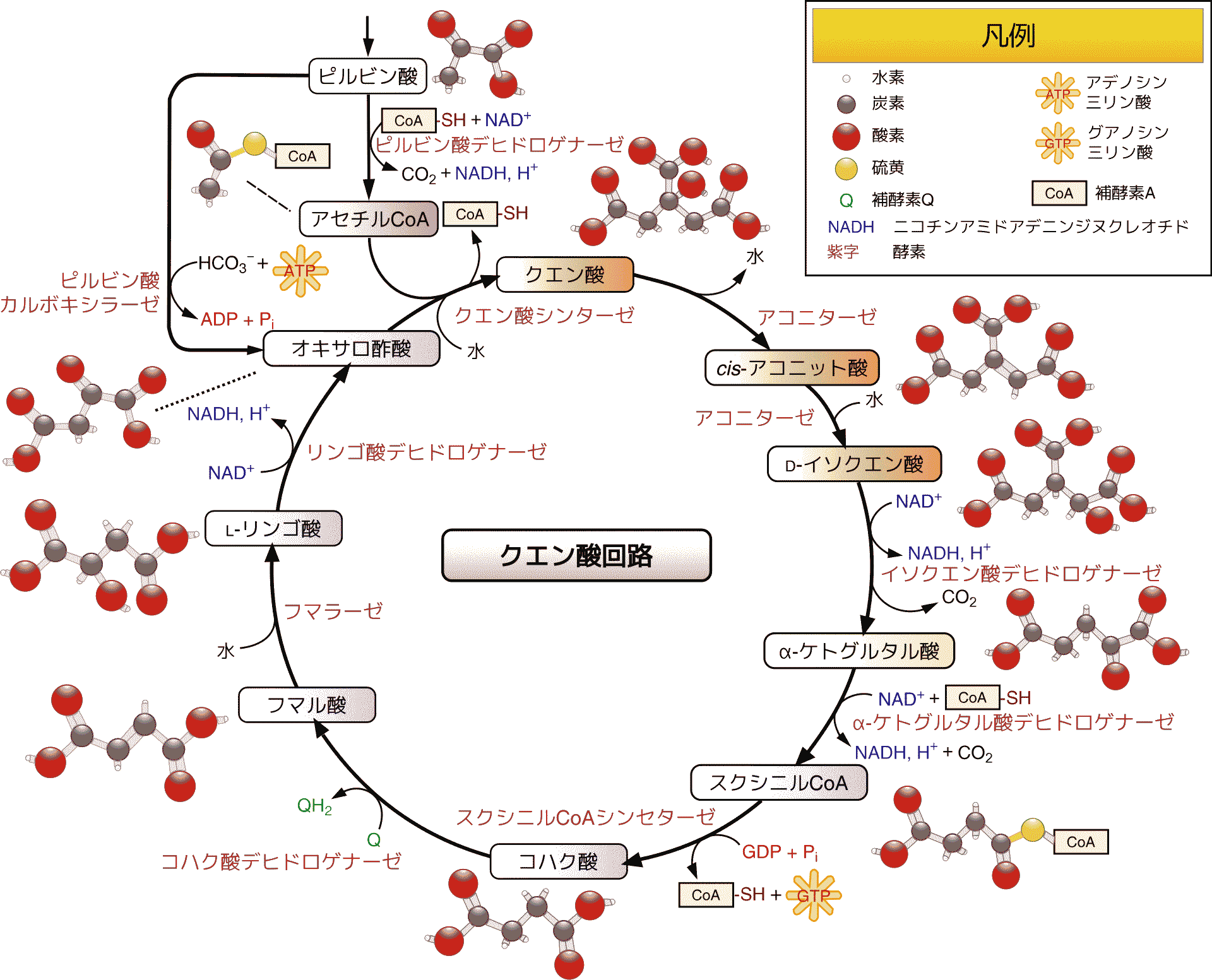
グリオキシル酸回路とβ酸化glyoxylate cycle and β-oxidationβ酸化 (β-oxidation)(CH2)nCH2·CH2·COOH↓________________↓ (CH2)nCO-SCoA___CHCO-SCoA (Acyl-CoA)________(Acetyl CoA)
動物ではミトコンドリア、植物ではグリオキシゾームで主に進行する反応でFpH2, NADH2が生産される
FMNH2 + O2 → FMN + H2O2 グリオキシル酸回路 glyoxylate cycle植物と一部の微生物が持つ(動物にはない)TCA回路変形 → TCA回路はミトコンドリア中で、グリオキシル酸回路はグリオキシゾーム中で行われる 脂肪酸を炭素源としアセチルCoAの形で利用する回路。種子発芽では、光合成により糖を獲得できるまで種子中貯蔵脂肪を利用し成長するため盛んに使われる回路
_________ Acetyl-CoA → Succuiante (C4) + NADH + H+ + 2CoA-SH Malate synthase, Isocitrate lyase: CH3COOHで誘導される
植物微小器官microorganismsには局在するが動物には殆どない酵素 リンゴ酸-アスパラギン酸シャトル malate-aspartate shuttle
NADH + H+ + OAA → NAD+ + malate 哺乳類で発達 電子伝達系呼吸系と光合成系での電子伝達系の相違呼吸: エネルギー順位が高次から低次へ移動し、その放出エネルギー利用 光合成: 光エネルギーで一端高次エネルギー体作り低次に移る際にATP生成 酸化的リン酸化 oxidative phosphorylation主にミトコンドリア内で行う反応系(ミトコンドリア単離成功後研究盛ん)呼吸鎖におけるエネルギー共役過程。この共役によりO2の電子輸送から得られるエネルギーを用いADPとリン酸からATPを生成する過程。即ち、酸化反応とATP合成の共役的な反応 機能1. 酸化的リン酸化により自由エネルギーはATPに貯蔵 = 酸化的リン酸化最終産物はATP
ΔG0' = -nF × ΔE0'
インタクトで自然なミトコンドリアの隔離を行う。Fluoride(enolase 解糖系酵素)を阻害 電子伝達系の解析電子伝達系解析にNADHを基質としてミトコンドリア内部に与えたいが、一般にミトコンドリアの膜に対しNADHは不透過
水処理をしたミトコンドリアを用いるとNADHは基質としての能力を持つようになる。NADPのP/O比は2-3
図. 電子伝達系 (♦: 阻害部位) 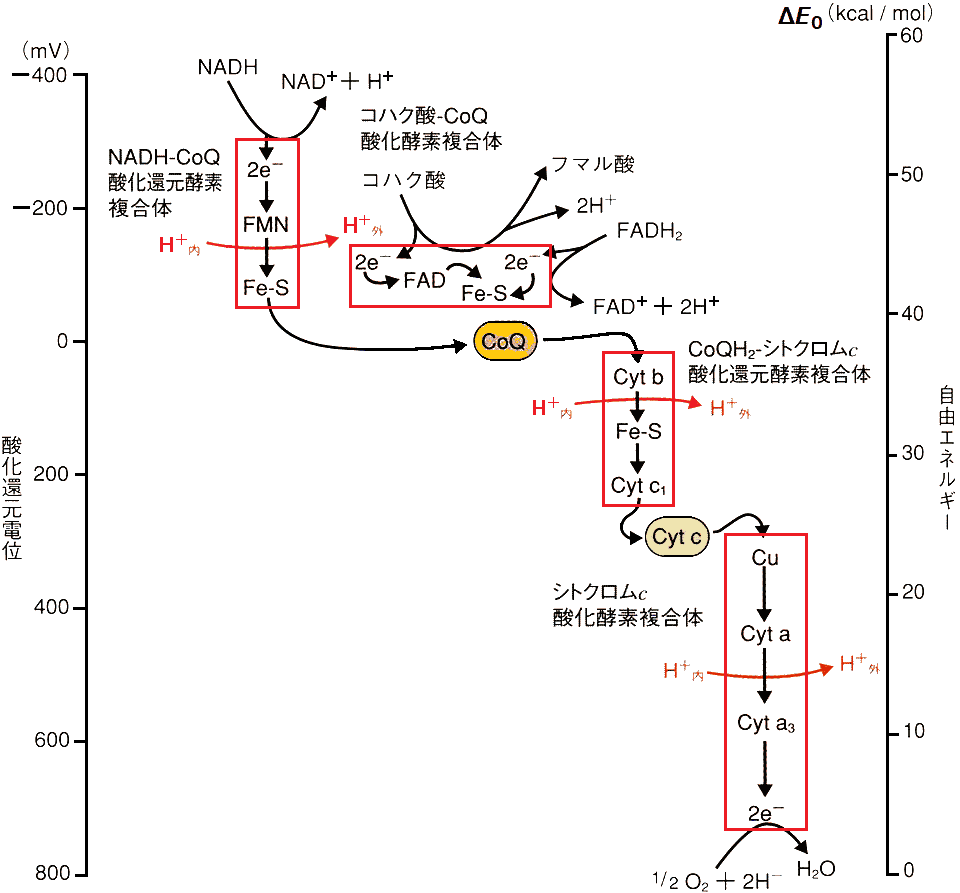 図. NADH, コハク酸, FADH2からO2への電子伝達 Ex. アスコルビン酸ascorbic acidを基質とすると生成される ATPは1である
NADH + H+ → cyt b → cyt c → cyt aa3 → O2 ミトコンドリア(主としてチトクローム cytochromes)と酵素Electron transfer unit particle (ETUP): 亜粒子を再構成する、つまり機能回復させることで酵素構造と機能の関連を調べる方法。電子受容体(electron acceptor, EA)を用い、これらのサブユニット中の酵素が調べられる
EA: Mbに対して、phenazine methosulfate(PMS), 2-6-dichlorophenol indophenol(2,6-DCIP)など
AH2 + NAD+ → A + NADH + H+
FMN or FAD (補欠分子族として働く)
脂溶性: ミトコンドリア膜に溶け込む
Hemeを持つ__Cytochromes
Fe2+: protoporphrin complex (Heme), Fe3+: protoporphrin (Hemin)
Cyto- 還元状態で示す吸収帯 酸化還元電位 分子量
chrome Heme α β γ E0'(V)
b protoheme IV 563 532 429 +0.03 30000
c1 heme C 554 524 418 +0.0225 370000
c heme C 550 521 415 +0.215 13000
a heme A 598 439 +0.19 ↑
a3 heme A 603.5 443 +0.385↓ 240000
Heme type (Heme group)
Heme A, Heme B: 非共有結合 ⇒ 酸性アセトン・酸性メチルコチルケトン 植物(wheat germ)のCyt. cのアミノ酸数112個。動物は大抵104個で植物Cyt. cのN端から8個のアミノ酸がとれたもの。他の植物では111個であり、これはC端からアミノ酸がwheat germからとれたもの Cytochrome b: ミトコンドリアと硬く結合分光光度計で液体窒素(liquid N2)をかけた77°K吸光は室温と比べて短波長側によりピークが複数になる
_____________b-556___b-560___b-565 サトイモ科 Cyt b7, b-557: autooxidation(酸素接触で酸化される)。シアンに呼吸阻害されない(CN--insensitive respiration)。Cyt b7に積極的な機能に関する知見ないが、器官が分解しなかったときに働く(仮説) Cytochrome a, a3: Cytochrome oxidaseとし機能
a, a3は結合した1つのオリゴマータンパク質
(a + a3)CN complex M.W. = 240,000: 7サブユニットからなる [ミトコンドリアDNA由来サブユニット + 核DNA由来サブユニット] Pigment 450 (P-450): COと結合すると450 nmに特異的ピークバンド表れる
動物肝細胞マイクロゾームで最初発見 - 解毒作用detoxificationに関与 |
ミトコンドリアとATPアーゼ(ATPase)1977 Racker E: ATPアーゼ(ATPase)のF1 (coupling factor 1)は、バクテリアのような酸化的リン酸化を行わない生物にもある。全体の分子量・サブユニット(5-6個)の分子量も高等生物とそれほど違わない
ATPaseを精製するとオリゴマイシン感受性 oligomycin sensitibityが消失する。ところがOSCP(オリゴマイシン感受性付与因子, oligomycin sensitibity conferring proein)を入れると、再びオリゴマイシン感受性が出る
βサブユニット__→ 触媒反応をつかさどるサブユニット 精製したF1は低温にするとサブユニットが分離し失活する(cold lability) ATPアーゼ (ATPase)のF0膜共有部分で疎水性が強く精製の難しいタンパク質N,N'-dicyclohexylcarbodimide (DCCD, binding protein) → クロロフォルム・メタノールで抽出 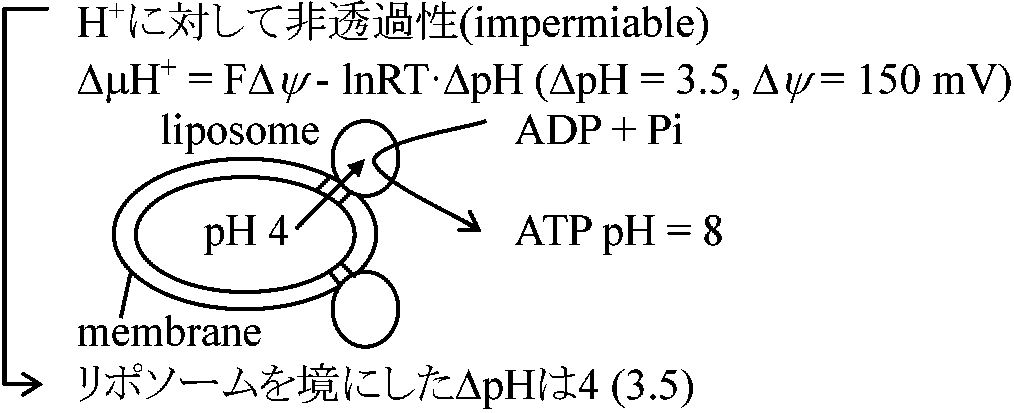
↑ リポソームは非透過性であるがF0を組み込むと透過性になる FFリポソームにおける人工的ΔμH+付与によるATP合成 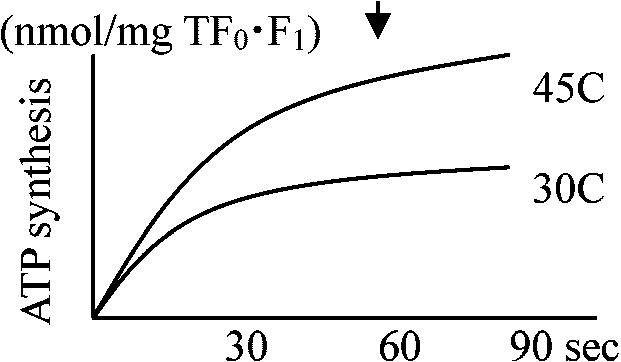
酸化的リン酸化機構 mechanisms of oxidative phosphorylation電子輸送の酸化還元エネルギーに必要なATPのリン酸化結合エネルギーへの変換過程、即ち酸化還元エネルギーからリン酸結合エネルギーへの転換機構には不明の点が多い。以下の3つの仮説(エネルギー中間体説・化学浸透圧説・膜構造変化説)は互いに排他的なものではない1. 化学共役仮説(化学説) chemical hypothesis (Slayter提唱)
Glycolysis … 可溶性solubleの部分で行われる
↓ A~X__AH2 + X + B ⇔ A~X + BH2__(| 2,4-DNP)
A: 電子運搬体electron carrier含む, X~Y: 電子運搬体を含まない高エネルギー中間体
ミトコンドリア膜 → H+ 不透過性 ⇒ 膜内外でプロトン濃度勾配(H+ gradient)生じる
酸化還元反応のエネルギーがタンパク質の高次構造に、即ち、電子担体あるいは共役因子分子のコンフォメーション変化という形でエネルギーが保存される NADP調達1. 解糖系glycolysisから: 解糖系の場合glycogenが基質carbohydrate →→→→ NADH 1'. 無機呼吸: O2を使わず呼吸物質を分解しNADP調達
基質: glucose, mannnose, amino acids, etc. C6H12O6 → 2C2H5OH + 2CO2___________ΔG0' = -54 kcal
C6H12O6 →→ 2C3H4O3 + 2CO2 glucose (C6H12O6) → 2C3H6O3__________ΔG0' = -47 kcal
C6H12O6 → → 2C3H4O3 → 2C3H6O3 (乳酸) C6H12O6 → n-C3H7COOH + 2CO2 + 2H2___ΔG0' = -15 kcal ラク酸菌 2ATP ΔG0' = 14.3 kcal
∴ 14.3/47 × 100 = 31%, 14.3/54 × 100 = 27%
発酵 fermentation: 呼吸生成物が人間生活に有用な場合 呼吸調節反応速度調節: C6/C1 ratio - グルコース端をラベルし調べたPentosephosphate pathway_CO2__glc.C-1___グルコースのC-1の炭素が脱炭酸 Glycolysis_______________CO2__3,4-C(pyt)_3と4位置の炭素が脱炭酸 TCA ①_________________ CO2__2,5-C(ac)_ 2と5の位置の炭素が脱炭酸 ____②_________________ CO2__1,6-C(ac)_ 1と6の位置の炭素が脱炭酸 _____________________initial CO2 C6/C1 ratio_低い → carbohydrate代謝はpentose phosphate pathwayが働いている __________高い →________________glycolysis~TCA cycleが働いている これはInitial CO2でなければこの値に信頼性なく、一つの目安にすぎない
細胞に必要な生合成物質、エネルギーが代謝の連続性metabolic sequenceを決定する。また、反応速度はATP, ADP, AMP, NAD+, NADHを介して調節される
細胞内のADPがすべてATPとして存在する - チャージ完全 エネルギーチャージによってアデノシンリン酸合成の方向がわかる 呼吸のStates 3, 4における ATP, ADPとvelocityの関係は裏づけの一つである。 Pentose phosphate pathway(PPP)の調節
G-6-P dehydrogenase(NADP+によって活性化、NADPHによって阻害される)の段階 呼吸制御比NADH + H+ + 3ADP + 3Pi + 1/2O2 → NAD+ + 3ATP + 4H2O受容体 acceptor ⇒ acceptor control 酸化反応速度がリン酸化反応の受容体(COの場合ADP)量により調節 → ADPが酸化反応全体の律速段階
呼吸状態(state): 1, 2, 3, 4, 5 脱共役剤uncouplarによる呼吸調節
P/O ratio: 酸化的リン酸化により得たATP合成のmol数とO2の消費されたグラム原子数の比
= 消費される酸素1原子につきADPのリン酸化に使われる無機リン酸の分子数 トリカルボン酸回路の酸化段階におけるP/O比Pyruvate (ピルビン酸) → Acetyl CoA (アセチルCoA)____________P/O=3Pyruvate + NAD+ + CoA-SH → Acetyl CoA + CO2 + NADH + H+ Isocitrate (イソクエン酸) → α-ketoglutal acid (α-ケトグルタール酸)__P/O=3Isocitrate + NAD+ → α-KG + CO2 + NADH + H+ Succinate (コハク酸) → Fumarate (フマール酸)________________P/O=2Succinate + Fp → Fumarate + FpH2 α-KG → Succinate______________________________________P/O=4
α-KG + NAD+ + CoA-SH → Succinyl CoA + NADPH + H+ + CO2
Malate + NAD+ → OAA + NADH + H+____________________⇓
2,4-DNP, CCP: 脂溶性。分子内に2重結合を有する弱酸(酸性基を持つ) CCP(カルボニシルアニドフェニルヒドラジン)
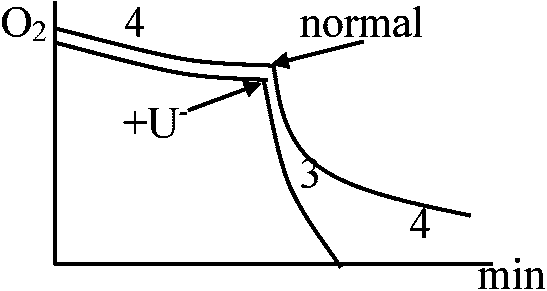
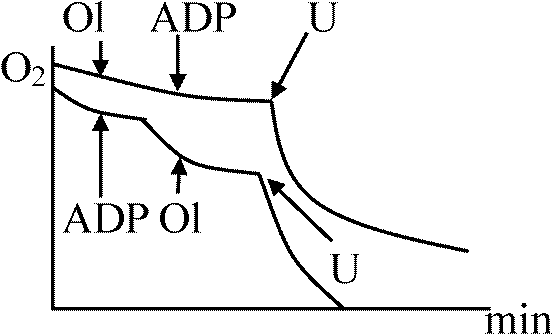 a) 脱共役剤をいれると高エネルギー状態high energy stateがなくなる → ADP欠乏時には酸素吸収速度が増大 b) Ol: oligomycin
high energy stateは見られるが: ADP →×→ ATP この共役を阻害
バリノマイシンvalinomycin、ナイジェリシンnigericinは、本来不透過なイオンを膜に対して透過可能にする物質。ある種の一価陽イオンがある時のみ高エネルギー中間体を破壊して透過できるようにする。したがって、普通ミトコンドリア膜に不透過である例えばプロトンイオンなどの膜透過を可能にする 部分反応 (partial reaction)1. ATPase
ATP + H2O → ADP + Pi AMP~P~☆P + Pi → AMP~P~☆P + Pi__阻害剤 2,4-DNP, oligomycin 3. Pi~H2O exchage (リン酸-水交換反応)HPO4 + H2☆O → HP☆O4 + H2O___________ 2,4-DNP, oligomycin 4. ADP~ATP exchange (ADP-ATP交換反応)AMP~☆P + AMP~P~P → AMP~P + AMP~P~☆P______________ 2,4-DNP, oligomycin 酸化的リン酸化反応は可逆的である→ 電子伝達系の可逆反応 reversibility of phosphorylation electron transport 動物と植物の代謝の違い貯蔵物質・二次代謝産物等に植物特有のもの多い
熱呼吸1778 Lamark: サトイモ科植物は開花時に熱上昇(呼吸盛ん) = 熱呼吸
この呼吸はCN耐性で、アンチマイシンantimycin耐性も示す 機能(説)1) 揮発性物質蒸発 → 昆虫誘引 pollinationAraceae (e.g., Arum italicum) 火焔苞 = 花序成熟時25°C温度上昇: 臭分散 + 訪花性昆虫活動活発化 2) 開花時寒冷対策
春植物 snow plant, Ex. Soldanella alpine L.
レタス: CN促進 加齢 agingEx. Strawberry leaf - 赤外ガス分析器によって同じ葉の成長を追跡
*: オルガネラ破壊により秩序だったエネルギー生産がずれ一次的に呼吸量上がる → climactericな呼吸 Fraxinus niger枝における呼吸の強さ
Tissue________Phloem__Cambium__Sapweed(白種) 窒素単位では動物と大きな差はない。窒素(タンパク質)単位と生重単位ではこれだけの値の違いがある 環境 environment1. 温度 temperatureQ10 = [rate at (t + 10)]/[rate at t] ≈ (一般に) 2
温度10°C上昇 ⇒ 呼吸速度約2倍(0-20°Cの間の時)
温度 (°C)____________________0_____10____20____30
温度変化と呼吸速度の関係
葉: 開葉直後最大 → 減少 → 夏季安定 → 温度低下に伴い減少(Q10 + 葉齢) 多くは気温10°C以下で低温感受性chilling sensitivity傷害応答起こる。酵素はそれほど失活していず、膜系が寒冷に弱く傷害が起こると考えられている Nitroxide compounds
Ex. 16-nitroxide methylstearate: CH3-CH2-C-(CH2)14-COOCH3
高濃度CO2は顕著な呼吸阻害 → 標準大気組成(0.03%)を大きく越える時にのみ阻害 大気中: 約21%の酸素 ⇒ 一般に、酸素に対する親和性affinityは高く微量酸素で飽和され、5-10%の酸素濃度があれば呼吸低下はない チトクロームオキシダーゼ cytochrome oxidase, thermal oxidaseHemeを持つ(Fe, Cu)。COおよび光の影響を受ける
Sugar Skunk Potato Rice Lemon V1/2: 50%阻害時のO2濃度 Apple seedling:
発酵解消点 (EP, extinction point) → パスツール効果 パスツール効果 Pasteul effect: グルコースに対する酵母の成長重量はO2が存在すると増加する。その結果、発酵は抑制されCO2放出がなくなり解糖作用のみが起こり、一定量のCO2放出が観察される 傷害応答 wounding response植物器官に切断等の傷害発生時の呼吸増大1) Phenol oxidase: 傷つけると基質のphenolとphenol oxidaseが作用しキノン生成。その時にO2吸収起こり呼吸量増大。キノンは重合し切断面を覆っていく作用があり、さらに殺菌作用を持つことが多く傷害回復に有用。キノンのコーティング作用の例としてリンゴの傷ついたところが茶褐色に見えるものがそれである 1) phenol oxidase
3) 脱分化(カルス化): 活発な細胞分裂が起こるため呼吸が増加する
一般に、傷害に伴う呼吸増大反応はシアン(CN-)に非感受性である Terminal oxidase1) Cytochorme oxidase2) Phenol oxidase: 植物の老衰期によく起こる
AH2↘↙Quinone↖↗H2O
ascorbic acid oxidase
AH2↘↙ NADP ↖↗_GSH ↘↙DHA↖↗H2O
H2O2 + H2O2 → 2H2O + O2
Ex._______________________ascorbic acid oxidase┇ O2 ATP Active Sensitivity Light
affinity 合成 center --------- reverse
共役 CN SO
Phenol oxidase 1.3×10-5 - Cu2+ + + -
Ascorbic acid oxidase 1.5×10-4 - Cu2+ + -
Glycolic oxidase ca 10-4 - FMN - -
Cytochrome oxidase 4.5×10-6 ++ Fe2+, Cu2+ + + +
Cytochrome by-pass high + Fe2+ - -
oxydase
|
|
植物: 光照射 - 通常呼吸(酸化的リン酸化)と異なる方法でO2消費しCO2生成 低CO2濃度、高温等の条件下 - 光呼吸速度が光合成速度を上回る場合 = 光呼吸によるCO2放出量が光合成のCO2固定量を上回る 6CO2 + 6H2O ⇔ C6H12O6 + O2
呼吸と光合成という逆反応が常に行われ光がある時に呼吸量測定困難 Rd = 暗呼吸 → 式が成立すれば光呼吸存在しない 1952-54 Brwon: Chlorella pyrenoidasa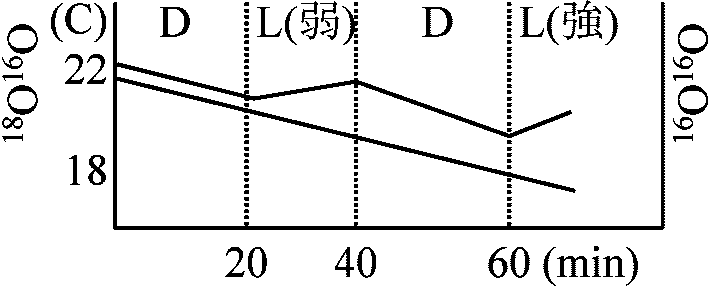
気相 18O, 16O(質量34)でラベル → 光合成に利用されない(呼吸のみ利用)
CO2, H2O: ラベルされていない
⇒ CO2放出速度が光照射停止直後著しく高く、暗中で急減。数分後に暗中の呼吸速度(呼吸量)と等しくなる
C4植物は補償点高______________ 暗呼吸 [O2] 20%で飽和 最大光合成高 C3植物は補償点低 |
RuBP carboxylase, glycolate oxydaseはcytochromeに比べO2との親和力が小さく飽和しにくい(後明らかに) 1966 Forester: 光呼吸(photorespiration)提唱1966 Zelitch: glycollateは代謝促進/光呼吸促進 = 条件同じ
→ 光呼吸基質はglycollateと推定
⇒ グリコール酸経路glycolic acid pathway発見 = 光呼吸 リブロースビスリン酸 ribulose bisphosphate carboxylase= カルボシキジスムターゼ (RuBP carboxylase/oxydase, rubisco)リブロース-1.5リン酸とCO2から2分子のグリセリン酸-3-リン酸を生成する反応を触媒する酵素 Mgイオンで活性化される。植物中に多量に存在し緑葉総タンパク質の約1/2を占める。フラクションIのタンパク質は大部分がリブロース2リン酸カルボキシラーゼからなり、タンパク的には同じと考えてよい。MW = 300,000, 17S。特にC4植物では維管束細胞中の葉緑体に局在する 1971 Bowes et al. グリコール酸がRuBPの酸化反応によりホスホグリコール酸を経て生じることを証明 2反応系がある1) CHOP-CO-(HCOH)2-CH2OP + CO2 → COOH-CHOH-CH2OP × 2分子 ____(main)_____________(RuBP)_____________________(PGA) 2) CHOP-CO-(HCOH)2-CHOP + O2 → _____(sub)
COOH-COOH-CH2OP + COOH-CH2OP 光呼吸: 電子伝達系と無関係。直接O2取込む = エネルギー・還元力共になし
光阻害・光傷害防御(決定的生理作用不明) |
|
= 生命維持に直接関わるといい難い(と初期には思われていた)が間接的に寄与する代謝の総称 = 個々の植物らしさを表す代謝 ⇔ 一次代謝 = 生命活動維持に直接必要(呼吸・アミノ酸・脂質代謝等) ゴムノキはゴムを、タバコはニコチンを作らなくても生存でき、これらの物質は個体生存には生理的に直接必要ではないが生産している。タバコ(ナス属)はニコチンを根で生産し導管を通じ地上部に転流する。ニコチンの葉中蓄積量は乾物重の数%にも達する。しかし、ナスの基部にタバコを接木するとニコチンを殆ど生産しないがタバコの成長に殆ど支障なく、ニコチンは隔離された環境では生命活動に直接は寄与しない。しかし、発芽60日目のタバコは1日約35 mMの炭素を同化したうち10数%をニコチン生産に回す二次代謝系の産物や中間体は化学構造が複雑で多岐にわたるが、生化学的手段(放射性同位元素を用いたトレーサー実験・酵素化学的実験)により合成経路の全貌はほぼ明らかとなった 二次代謝産物 secondary metabolite二次代謝によって得られた生体物質1. 生合成経路に基づく = イソプレノイド、ポリケチド等 2. 構造的に雑多でも共通特性を有する= サポニン、タンニン、アルカロイド等 - 慣用名多 炭水化物 ←─ [光合成] ├────┐ ↓ │ [解糖系] [ペントースリン酸回路]──┐ ├────┘ エリトロース- ←┘ ↓ ┌─4-リン酸 ホスホエノール─┴(シキミ酸経路)─→芳香族──┬→[フェニル ピルビン酸 アミノ酸 │ プロパノイド] │ └→[リグニン] │[クエン酸回路]→脂肪族──→(アミノ酸回路)─→[アルカロイド] │ │ アミノ酸 ↑ ↓ │ └───────┬→[フラボノイド] アセチルCoA ┬→マロニルCoA →(ポリケチド回路)┴→[芳香族ポリケチド] └→メパロン酸─→(メパロン回路)──→[イソプレノイド]一次代謝と二次代謝の関係
シキミ酸経路 (shikimic acid pathway, SA)1885 Eykman: 発見1937 Fischer HOL: 構造決定 1950's 立体構造決定 de novoに可能
炭素の由来14C-Glc → SA: SAに14Cは入る - SAのどの部位にどの経路から入るか1954 Sprinson & Davis: E. coli 83-24 - 取込実験で直前前駆体収率調べる
D-glu-6-P, D-Frc-1, 6-P2, D-rib-5-P 5% シキミ酸生成(1)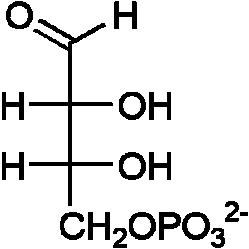 ⇒ H2O↘↗PO43- ⇒
(2)
⇒ H2O↘↗PO43- ⇒
(2) 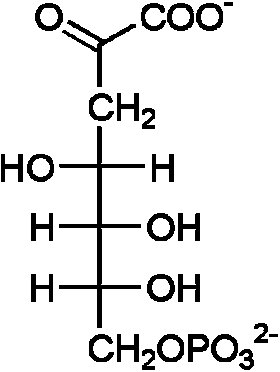
(1) ホスホエノールピルビン酸 + エリトロース 4-リン酸 → (7-ホスホ-2-デヒドロ-3-デオキシアラビノヘプトン酸アルドラーゼ) → 7-ホスホ-2-デヒドロ-3-デオキシアラビノヘプトン酸 + リン酸 ⇒ NAD+↘↗NADH ⇒ (3)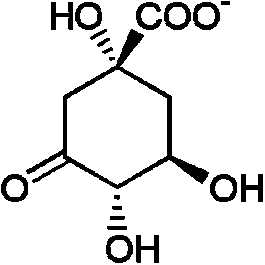 ⇒ ↗H2O ⇒
(4)
⇒ ↗H2O ⇒
(4) 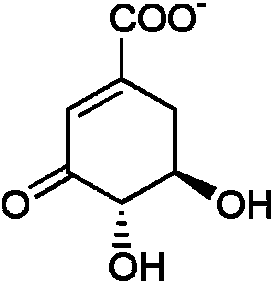 ⇒ ⇒
(2) 7-ホスホ-2-デヒドロ-3-デオキシアラビノヘプトン酸 + NADH 3-デヒドロキナ酸シンターゼ (EC 4.2.3.4) → 3-デヒドロキナ酸 + リン酸 + NAD+ (3) 3-デヒドロキナ酸 → 3-デヒドロシキミ酸 + H2O 3-デヒドロキナ酸デヒドラターゼ(EC 4.2.1.10) (4) 3-デヒドロシキミ酸 + NADPH → シキミ酸 + NADP+ シキミ酸デヒドロゲナーゼ (EC 1.1.1.25) NADP↘↗NADP+ ⇒ (5)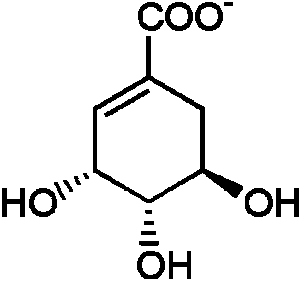 ⇒ ↗H2O⇒
(6) ⇒ ↗H2O⇒
(6) 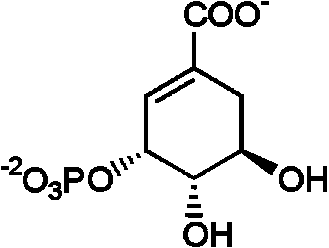
(5) シキミ酸 + ATP → 3-ホスホシキミ酸 + ADP シキミ酸キナーゼ (EC 2.7.1.71) (6) 3-ホスホシキミ酸 + ホスホエノールピルビン酸 3-ホスホシキミ酸1-カルボキシビニルトランスフェラーゼ(5-エノールピルビルシキミ酸-3-リン酸シンターゼ) (EC 2.5.1.19) → 3-ホスホ-5-エノイルピルビルシキミ酸 + リン酸 ⇒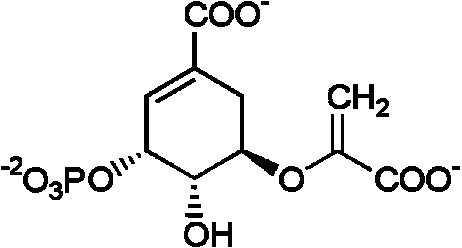 ⇒ ↗PO43- ⇒ ↗PO43-
(7) 3-ホスホ-5-エノイルピルビルシキミ酸 → コリスミ酸 + リン酸 コリスミ酸シンターゼ (EC 4.2.3.5) ⇒ (8)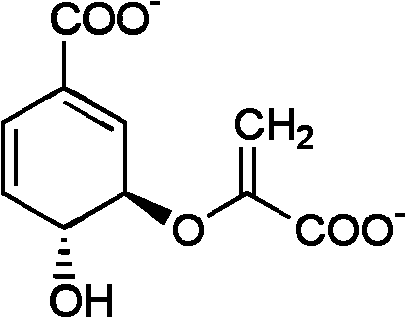 ⇒ ⇒
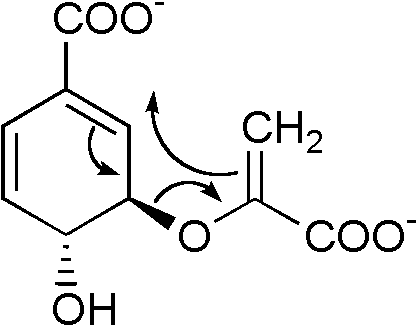 ⇒ ⇒
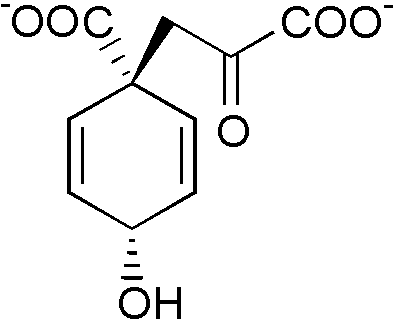 (8) コリスミ酸 → プレフェン酸 コリスミ酸ムターゼ(EC 5.4.99.5) 生合成フェニルプロパノイド合成フェニルプロパノイド: ベンゼン環に炭素3個の側鎖をつけたC6-C3化合物植物で、ヒドロキシ桂皮酸やそのエステルとして広く分布。クマリンに変換したりフラボノイドやリグニンの構成成分としても組み込まれる 合成経路: シキミ酸経路を経て生成するフェニルアラニンが出発点 フェニルアラニン → [脱アミノ基と水酸化] → 4-クマル酸(4-ヒドロキシ酸) = フェニルプロパノイド基本化合物 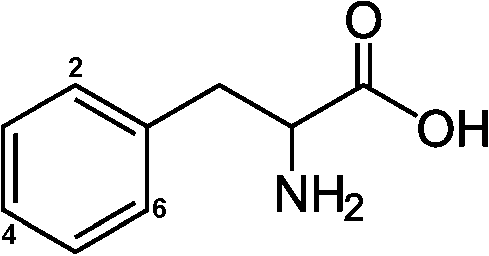 フェニルアラニン フェニルアラニン___↓ フェニルアラニンアンモニアリアーゼ(PAL) 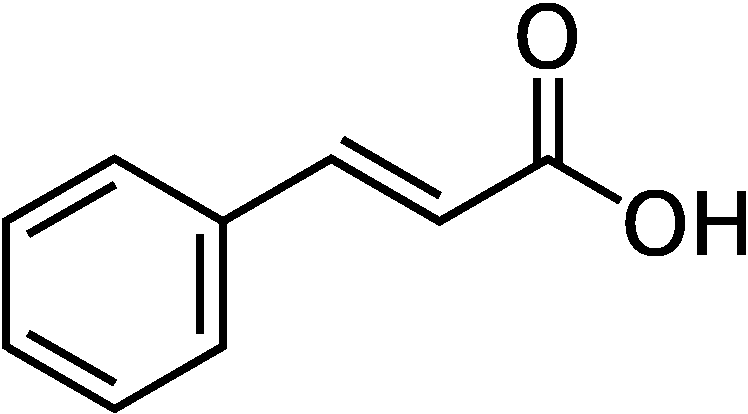 トランス-桂皮酸 トランス-桂皮酸___↓ 桂皮酸-4-ヒドロキシラーゼ 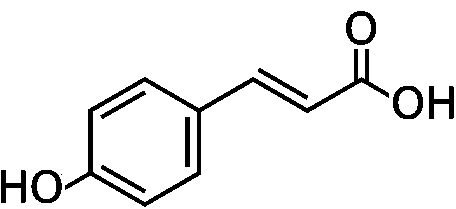 → → 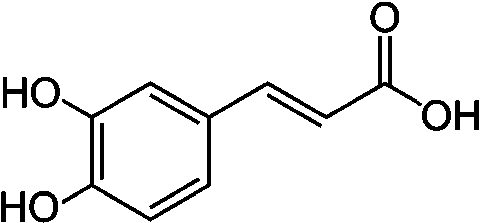 ______(↗ クマリン酸)
______(↗ クマリン酸)_______4-クマル酸____________カフェー酸_________⇒ (1) ______________________↓ ヒドロキシ桂皮酸O-メチル _______________________ トランスフェラーゼ 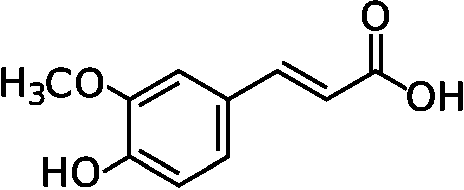 _____5-ヒドロキシフェルラ酸________フェルラ酸 ___↓ ヒドロキシ桂皮酸O-メチルトランスフェラーゼ 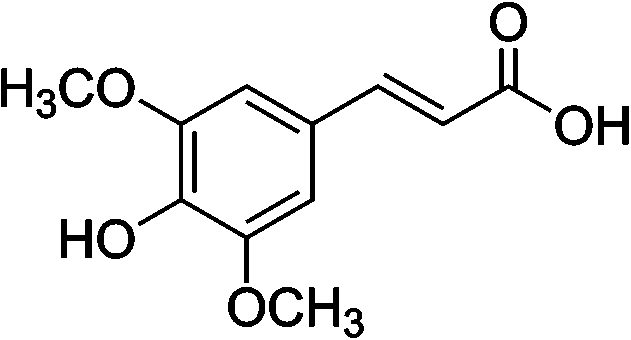 シナピン酸 シナピン酸 |
_________________(1) ⇒ 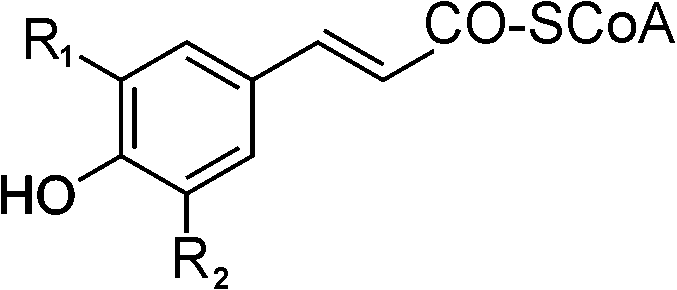 トランス-桂皮酸 トランス-桂皮酸ヒドロキシ桂皮酸: CoAリガーゼ(CL) ↓__ヒドロキシシンナモイルCoA _______ ┌───────────────┼──────┐ R1, R2: -H, -OH or -OCH3 ____フェノール酸/エステル類___フラボノイド___リグニン フェニルプロパノイドの代謝 ヒドロキシ桂皮酸類 hydroxycinnamic acid group: フェニルアラニンを脱アミノ化し桂皮酸を生成する。フェニルアラニンモリアーゼ(PAL)は、芳香族二次代謝に導入する最初の酵素であり、二次代謝産物の多くの合成量と高い相関を持ちながら活性レベルを変動させており二次代謝の流れを左右する律速酵素と考えられる。合成されたヒドロキシ桂皮酸類がリグニン・フラボノイドなどに導入されるためには、CoAエステルとして活性化されねばならないクロロゲン酸 chlorogenic acid: 桂皮酸類がグルコース・キナ酸・シキミ酸等の水酸基持つ化合物とのエステルとし存在 Ex. ヒドロキシシンナモイルCoA クマリン coumalin or coumarin: セリ科・ミカン科に広く分布する植物香料の一種。一般に細胞伸長・種子発芽阻害する生理活性ある
生葉: クマリン酸(o-クマル酸)配糖体とし液胞内 - 無臭 リグニン lignin ゴム: ポリテルペンとしてアセチル CoAから作られる
天然ゴムnatural rubber: 熱帯ゴムノキ樹液が原料 → アレルギー(アナフィラキシーショック)
特色: 植物体内での含量変化が著しい → 植物の成育に関係 人体致死量: モルフィンで2mg/kg、苦味を有する劇毒のストリキニンで0.75mg/kg
植物アルカロイドは数種のアミノ酸を前駆体として生合成される
窒素を含む複素環を持ち有機酸と結合し存在するが、ほとんどは構造複雑で光学活性なため構造
双子葉植物に含む種多く、1個体に多種類のアルカロイドが共存する プロトアルカロイド: 異項環を含まないもの プシュウドアルカロイド: 含窒素塩基だが炭素骨格がイソプレノイドやポロケチド類に由来
二次代謝産物の機能生存競争植物・微生物で数多く発見(動物稀) → 二次代謝産物の多くが他生物に対し何らかの生理的作用動物捕食回避による生体防御物質 Ex. ゴム・精油・アルカロイド・アントシアン・タンニン → 動物との共進化 1976 Seigler & Price: 二次代謝産物は静的な代謝最終産物ではなく動的平衡状態で植物体内に存在する⇒ 代謝産物の転換時間短く、他の重要代謝過程の中間産物でもある 動物: 自然淘汰に大きく関与するのは運動性植物: 非運動性の植物が生物間相互作用を通じ生き延びるには運動性に代わる手段を用いなくてはならない 共進化coevolution・相互作用interaction進化 → 二次代謝発達 化学生態学 chemical ecology生物が放出する化学物質を介する生物間相互作用を研究Ex. アレロパシー物質、フェロモン、二次代謝産物 アレロパシー (他感作用, allelopathy)Def. 植物が化学物質を放出し、他植物成育に影響 ☛ 生物学的侵入= エチレン・テルペン類等揮発性物質。帰化植物が良く生産 (-) 連作障害一因 vs (+) 生物農薬(雑草防除) 1936 Molisch (1922-1925 東北帝国大学主任教授)リンゴをガラス鐘で覆いトマト鉢入れるとトマト葉縮れる ☛ エチレン アレロケミクス allerochemics: 異種生物に作用するアレロパシー物質の総称物質機能: 誘因、摂食刺激、産卵刺激、忌避、攻撃・防御(有毒) 1. 植物 ⇔ 大型哺乳動物 草食動物への防御作用 → アルカロイド・タンニン1975 Hovin & Merten: Phalaris arundinacea
グラミン gramine, トリプタミン tryptamineの2種類のアルカロイド生産
⇒ 病害虫の発生しやすいところにアルカロイド植物多 1976 Futuyma: キノン、サポニン、アルカロイド、シアン配糖体樹木より草本の方に多く発達 2. 植物 ⇔ 昆虫昆虫忌避作用 → テルペン vs. 昆虫誘因作用 → フラボノイド・精油 マツ科植物と昆虫ホルモン エクジソン (ecdysone、脱皮ホルモン/前胸腺ホルモン) 1965: 化学構造決定: 2.5 mg/(500 kgカイコ蛹)抽出 1966: Taxus baccataから抽出 → 25 mg/25 g (葉/根)という高含有率で抽出可能となる シダの1種の根茎2.5 mgから25 μg抽出 → 食害防御物質 → 様々な植物から発見 = phyto-ecdysoneと命名裸子植物やシダに多 - 共進化の典型的な一証拠 偽幼若ホルモン: ホシカメムシ飼育中、南米から合州国へ運ぶと5令幼虫で成長停止となる異常発生
使用台紙: 南米 = ワットマン濾紙 ↔ 合州国 = スコットペーパータオル
アレロパシー: 他生物の成長を抑制阻止する物質を出すこと クルミ walnut: 葉でjugloneを生産 → 雨露で地上に落ちると多くの周辺植物の成長阻害 ケンタッキーブルーグラス: 阻害を受けない
カシoak: Salicylic acid生産
ブタクサ等の他種成長を抑制 病原体への抵抗作用 → リグニン・タンニン・フィトアレキシン preinfectional compounds: キノン類・タンニン → Juglone postinfectional compounds:
1) 結合型: 感染後freeとなる: cyanogen glycosides 2) 合成型: pisatin 生体防御 biological defense, biophylaxis耐性 tolerance: 食害を受けても高い再生力がある抗生物質作用 antibiosis + 忌避物質 non-preference: 二次代謝産物 構造的防御 structural protection: サボテンの刺、ヒイラギの葉縁の突起など ☛ 森林浴 フィトンチッド phytoncideExp. 植物(ニンニク等)を傷つける + 周囲に微生物懸濁液1摘
→ 微生物は死滅-麻痺 (仮説) 植物は傷つかなくてもフィトンチッド分泌 Exp. 葉に傷 → 負の走化性 (仮説) フィトンチッドは生体防御物質森林浴 forest bathing |
|
色素(顔料) pigment: 分子内に長波長光吸収する発色団 → 色呈する物質群
植物色素研究初期 = 染料色素分析 = 水溶性で安定なフラボン、フラボノール類が研究対象 1900年代: 生理学的に注目 Ex. クロロフィル、カロチノイド等の構造解明便宜的分類: フラボノイド系、キサントン系、キノン系、カロチノイド系、クロロフィル系、フィコビリン系、メラニン系等
(安田 1977) 四大色素 four major pigments0. 白: 白い色素は自然界に存在しない → 白花: 気泡が主な原因 = 光工学で意味する白色は自然界にない1. カロチン: 赤、オレンジ、黄色 花弁を始め植物の殆どの部分に分布(動物にもある) Ex. ニンジン、トマト,カボチャ、カキ
β-カロチン carotene: 最も多い |
2. フラボノイド flavonoid: 2フェニル基が3炭素鎖を介しγ-ピロン環(+類似構造)を作り結合したC6-C3-C6型化合物
フラボン + アントシアン
フラボン類 薄くなる 黄 濃くなる 中心子目(科: アカザ、ヒユ、オシロイバナ、ヤマゴボウ、ツルナ、スベリヒユ、ツルムササキ、ナデシコ、サボテン)が特異的に含む → 系統解析に応用 分布組織レベル: 花弁表皮部分集中。表皮近く柵状組織にも分布することがある細胞レベル: プラスチド: カロチン – 水に溶けにくいため 液胞: カロチン以外の色素 花色: pH説 (Willstatter): 花色はpHで変化
コピグメント(助色素)copigment説 (Robinson) 花色素 flower pigment花色を決める色素 - [起源] 花を作らないシダにある? |