(2025年9月29日更新) [ 日本語 | English ]
有珠山 / サロベツ泥炭採掘跡
1986年, 2006年の有珠山火口原. ワタスゲ・エゾカンゾウ
HOME > 講義・実習・演習一覧 / 研究概要 > 小辞典 > 生物・物質循環
[ 生物地球化学循環 | 窒素循環 | 農薬循環 ] [ 栄養段階 | 光合成 ]
地圏(geosphere)地球内部の空間↓ リソスフェア (岩圏, lithosphere) ↓ アセノスフェア (asthenosphere) ↓ メソスフェア (mesosphere) ↓ 外核 (outer core) ↓ 内核 (inner core) 水圏 (hydrosphere)水 (water) が構成する空間 ≈ 海洋 + 湖沼 + 河川大気圏 (atmosphere)地表を覆う気体の空間生物圏 (biosphere)生物が生息する空間 (s.l.) → 生物相(s.s., biota)生物群集 biocoenosis: 生物圏中の生物集団の意味で時々見る言葉 物質エネルギー循環 material and energy cyclesエネルギー energy: 生態系収支第1法則: 全生物は他の全生物と結び付く = 連鎖網証明実験(背理法): 仮に1生物単位を消滅させ、その後の生態系変化測定
Ex. 遷移: 湖富栄養化過程は、水中塩の急速な濃度上昇が藻類の急激な繁殖をもたらし、湖底への光浸透率低下 → 繁殖した下部の藻類は死滅し湖中有機廃棄物量増加し、この分解により水中酸素含有量は全体的に減少 → 酸素を必要とする分解バクテリア消滅し水圏バランス崩れる。1つの単位として成立する生態系への外部圧力はバランスを崩しやすい 第3法則: 自然が最もよく知っている → 研究と発展の必要性 requirement of research and development 天然システムへ人工的変化を与える = システムに対し害を与える 第4法則: 代価を払わなければ何も得られないDef. 自生的autochthonous物質: 群集内で作られた有機物/エネルギー ⇔ Def. 他生的allochtonous物質: 外部からその群集に運ばれた有機物/エネルギー 生態系のエネルギー移動 energy flow in ecosystem熱力学 thermodynamics1. エネルギー不変の法則: light → photosynthesis + heat ≡ Model equation: E1 → E2 + (heat or loss) 2. エントロピー増大の法則
あるエネルギーは常に分散し仕事をしない(=利用不可)エネルギーに変化 = いかなるエネルギーも潜在エネルギーに自然変換することはない |
エネルギー環境a. 生体エネルギーの源泉 = 1) 光合成、2) 無機物、3) 有機物
緑色植物: H2O + CO2 + light energy → Organic substrates
栄養段階 trophic level 光合成のエネルギー効率 efficiency生産者の光合成により有機物として固定される割合地表到達太陽光エネルギーの約半分が光合成に利用可能
2 gcal/cm2/min (theoretical) → 1.34 gcal/cm2/min (実際の利用量): 空気中のダスト等により減少 エネルギーの大部分は熱とし失われ、光合成利用されるのは植物吸収エネルギーの0.8-4%位 光エネルギーは光合成により化学エネルギーとなり有機物中に貯えられる。この有機物は食物連鎖を通じ生産者からより高次消費者へと渡され、各栄養段階で一部が熱エネルギーとして放出される。高次消費者に捕食されず死んだ個体の有機物も、分解者により無機物に変わり再び植物は利用→ 有機物に貯えられたエネルギーは分解者を含む各栄養段階で少しずつ消費され再利用不可能 機物を作る炭素・窒素・リン・イオウ等の物質は生態系中を循環する
熱帯
照葉
針葉
ススキ
富栄 * エネルギー効率 緯度差: 英国(N51°-59°): 2.5 × 108 cal/m2/day <
USミシガン(N42°-48°): 4.7 × 108 < Spitsbergen (80°N): 夏 1050, 冬 0 |
[海洋循環]
|
= 生物地球化学サイクル
地球規模の循環 = 物質移動を、大気圏-水圏-地圏-生物圏の間で見る 熱循環 (thermal cycling)水循環 (water cycle) = 水文学的循環 (hydrologic cycle) 大気循環 (atmospheric circulation) 海洋循環 (thermohaline circulation) 物質循環 (material circulation) 等 物質による循環区分窒素循環 nitrogen cycle酸素循環 oxygen cycle: 緑色植物光合成と、多生物の酸素呼吸通し循環 炭素循環 carbon cycle リン循環 phosphorus cycle: 生物体構成物質として重要
岩石風化による供給(主) → P, K, Ca, Mg溶出(イオン化) → 植物利用/菌根菌 水素循環 hydrogen cycle P, K, Ca, Na, Mg, etc.: 塩類として植物吸収 → 一部は食物とし動物に取込まれるが、最終的に遺体や排出物となり再び塩類に戻る 等 |
☛ 用語 POM: 粒子状有機物 particulate organic matter
CPOM: 粗粒状有機物 coarse POM
メンブランフィルター(0.45 μm φ)通過する全有機物 Precipitation = St + Pt + Ps
St (林内貯留): 樹冠により遮断された水量 → 蒸発
林冠構造により異なる
⇔ 林外雨incident precipitation: 接触なしに地表へ 林内雨の数%程度 → 樹幹上のイオンを溶かし地表へ |
[ 同位体 ]
|
同位体: 移動速度異なる =
移動あれば様々なスケールで安定同位体存在比(同位体比)変化 ⇒ 同位体比n個の同位体Iiからなる元素の原子量, Aw = Σi=1npiIi良く利用される同位体: H, C, N, O (水として), S P: 安定同位体がない = 使えない 植物体内物質移動同位体分別: 同位体の比率が変わること → 物質移動δ13C植物全体のδ13Cを決める要因
• C3植物 RubiscoがCO2と最初の反応: 12CO2を優先して触媒(分別高) C3植物 ≈ -27‰ (-30 to -25) ⇔ C4植物 ≈ -12‰ (-15 to -10) • C4植物 PEPカルボキシラーゼがHCO3-と最初の反応: 分別小森林: 強光浴びる樹冠葉は林床葉に比べδ13C値が高い 草原: 乾燥化に伴い蒸散抑制のため気孔閉じる → Δ↓ ⇒ 草原丘陵: 高地や斜面の葉のδ13C値は土壌水分の豊富な低地より高い 表. 光合成過程に関連する炭素安定同位体分別 (‰)
CO2の水への溶解 = 1.1 ↔ CO2の水和 = -9.0 |
水利用効率 (water-use efficiency, WUE)推定 WUE = A/E = Ca(1 - Ci/Ca)/(1.6·VPD)
A: 光合成速度, E: 蒸散
利点: 葉のセルロースは下位葉が固定した糖に由来 - 移動 - δ13C変化 葉内CO2拡散コンダクタンス推定δ15N: 窒素移動窒素固定植物: Nは土壌と大気から ↔ 非窒素固定植物: 土壌からのみ植物: 硝酸吸収ではN同位体分別殆どない ↔ 根・葉の硝酸還元では分別大 δ15Nを窒素固定をしない植物と比較し窒素固定由来窒素量を推定 植物サンプル試料: 60-80°Cで乾燥 → 40 μm程度に粉砕同位体組成は乾燥させれば分解起こらず殆ど変化しない 測定: 1サンプルあたり0.05mg/N程度必要
植物根: 土壌窒素含量によるが2-10mg δ18O, δD: 水利用生態系内・間物質移動炭素濃縮係数 0.8‰ - 餌資源を反映窒素濃縮係数(CN) 3.3-3.4‰ - 栄養段階を反映 栄養段階, tl = (δ15Ntarget - δ15Nstd)/CN + 1
target: 対象種 |
|
地球レベル → 穀物輸入 = 窒素移入 ⇒ 穀物輸入大国(Ex. 日本)に窒素集積 窒素 (N): タンパク質、核酸、葉緑素、ATP等の構成元素 植物の窒素取込、葉緑素合成には鉄が必要 → 海洋では鉄循環が重要 大気中79% = N2 → 特定生物以外は直接空中窒素を利用できない→ 土壌中可溶N (NH4+, NO2-, NO3-等)利用 → 食物連鎖 → 他生物へ循環
植物成長に光・水制限ない → 生産性は土壌中無機N量により規制 A. (空中)窒素固定 nitrogen fixation同化的硝化還元: 硝酸塩 → 亜硝酸 → アンモニア → 窒素を含む生体高分子1. 空中放電・火山活動生物非関与空中窒素固定雷等で化学変化が起こり土中にNO3-が供給される (工業的窒素固定含む) ☛ 根圏 2. 生物による窒素固定空中(遊離)窒素を直接利用し窒素化合物作る(原核生物のみ)
1986 Hellriegel: マメ科根粒による空中窒素固定証明
ニトロゲナーゼ nitrogenase a. 共生的窒素固定(一部土壌細菌) = 土壌微生物: 1 gの土に1億の微生物 i. 根粒菌 rhizobia, leguminous bacteria, root nodule bacteria マメ科植物と共生 一部共生的窒素固定菌は宿主を離れ独立性窒素固定菌として生育できるが大半は単独生存できない = 宿主特異性高
Rhizobium: R. melioti, R. leguminosarum biovar. viciae エンドウ菌
植物: 窒素が制限要因とならない
根粒中の根粒菌は根粒崩壊後土に戻る 根・(茎・葉)内部に窒素固定菌が生育する
Ex. サトウキビ等のイネ科植物、ヤシ、チャ、コーヒー ホスト不在なら単独生活可 放線菌根性植物 actinorhizal plants: 放線菌共生し空中N2固定植物
放線菌根 actinorhiza: フランキアが形成した根粒 (山中・高橋 2008)
Hippophae (サジー), グミ科, 果樹とし試験栽培
Casuarina (モクマオウ) Ex. C. equisetifolia, 防風林、沖縄・小笠原植栽
Podocarpaceae Ex. Podocarpus macrophyllus, Nageia nagi 絶対嫌気性細菌: 酸性土壌多 - 地質の比較的固いO2ない嫌気的環境 Clostridium, Desulfovibrio, Desulfotomaculum 通性嫌気性細菌 Ex. Klebisiella, Bacillus好気性: 中性土壌多 - O2が比較的多量にある好気的環境 Azotobacter, Azomonas, Beijerinckia 藍藻植物の一部 Ex. Nostoc, Anabaena, GloeocapsaB. 窒素同化 nitrogen assimilation無機窒素化合物(硝酸等)を有機窒素化合物(アミノ酸等)にする過程窒素分子(N2)は反応性乏しい 1. 硝化作用/硝酸化成作用 nitrificationa. NH4+ → [亜硝酸菌] → NO2- → [硝酸菌] → NO3-
アンモニア酸化菌(亜硝酸菌): Nitrosomonas, Nitorosococcus, Nitrosospira, Nitrosolobus, Nitrosovibrio |
Warington vs Winogradsky: 共に亜硝酸菌・硝酸菌単離試みる
1879-1888 Warington: 有機物を含む培地では単離できない → c. 還元型フェレドキシン(Fdred): 亜硝酸を6電子を使いNH3に還元
NO2- + 6Fdred + 8H+ → NH4+ + 6Fdox + 2H2O 2. アミノ化 amination最初のアミノ酸(amino acid)が作られる反応NH4+が呼吸中間物質のケトグルタル酸と結合しグルタミン酸 Glu になる過程 a. COOH-C(=O)-CH-CH-COOH (α-ケトグルタル酸) + NHDH + H+ + NH3 ⇔ [グルタミン酸脱水素酵素] → COOH-CHNH2-CH2-CH2-CH2 (L-Glu) + NAD+ + H2O b. COOH-CHNH2-CH2-CH2-COOH (L-グルタミン酸)+ COOH-C(=O)-CH-COOH (オキザロ酢酸) ⇔ [グルタミン酸トランスアミナーゼ] ⇔ c. COOH-C(=O)-CH2=CH2-COOH (α-ケトグルタル酸)+ COOH-CHNH2-CH2-COOH (L-アスパラギン酸) 3. アミノ酸合成 amino acid synthesisアミノ酸転移反応: 様々なアミノ酸ができる過程グルタミン酸のNH2基がトランスアミナーゼの働きで様々な中間物質に渡され様々なアミノ酸を合成 a. L-アミノ酸酸化酵素 FMN
COOH-CHR-NH2 + O2 + H2O → COOH-CR=O + NH3 + H2O2 c. COOH-CHNH-CH-COOH (L-アスパラギン酸) → [アンモリアナーゼ] → HCCOH=CHCOOH (フマル酸) C. 脱窒(素)作用 (denitrification)硝酸還元菌が硝酸態窒素を窒素ガス化 - 大気へ (普通土壌少、水田旺盛)硝酸還元 (nitrate reduction)/亜硝酸還元 (nitrite reduction)
NO3 → NO2 → (HNO)2 → NH2OH → NH3 NO3- → NO2- → NO → N2O → N2 微生物中にはガス状N2を作り出し放出するもの(脱窒素細菌, 脱窒菌)がある
Pseudomonas denitrificans, Paracoccus denitrificans 5S + 6KNO3 + 2H2O → K2SO4 + 4KHSO4 + 3N2 排出物質生成アンモニア化成作用(生成作用): 窒素循環中、動植物遺体・排出物等の有機窒素化合物が、土壌微生物に分解されアンモニア(NH3)に変化する過程プリン分解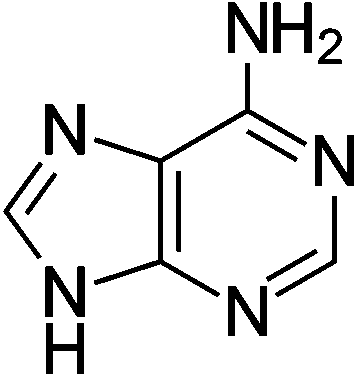 アデニン アデニン
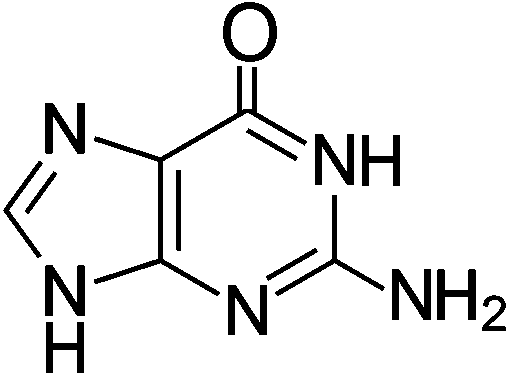 グアニン グアニン
↓ アデナーゼ ↓グアナーゼ 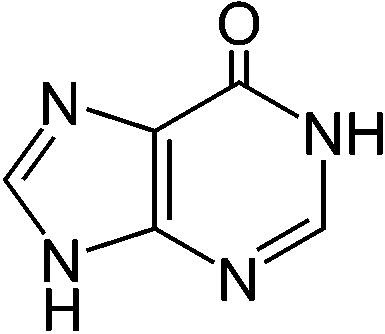 __→__ __→__
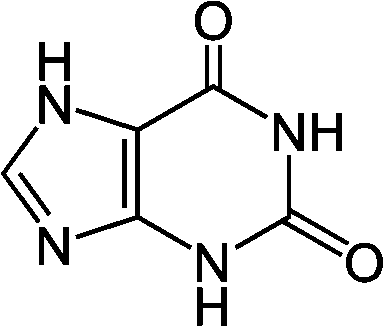 __→__ __→__
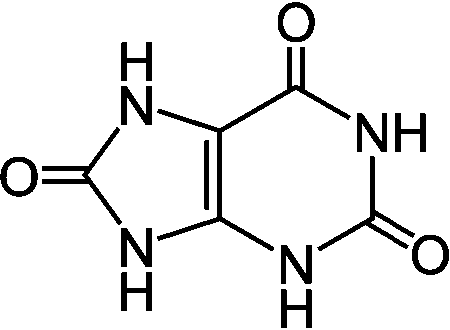
___ヒポキサンチン_____キサンチン_______________尿酸 _________________├ キサンチン酸化酵素 ┤_________↓ウリカーゼ 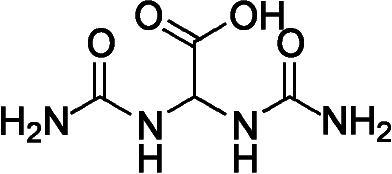 ←アラントイナーゼ← ←アラントイナーゼ←
______アラントイン酸___________________アラントイン __ ↓アラントイガーゼ CHO-COOH + CO(NH2)3 → CO2 + NH3 グリオキシル酸_尿素_├ウレアーゼ┤ NH3は細菌、菌類、放線菌が摂取利用 水田Def. 乾土効果(土壌乾燥効果) soil-drying effect: 土壌乾燥が植物成長や土壌物理・化学的性質に与える影響
水田乾土に水加えると微生物活性によりNH3発生 肥効高める(一時的) + 団粒構造崩壊、保肥力低下、土壌劣化リスク 地温上昇効果: 水田温度上昇すると無機化促進アルカリ効果: 石灰を加え湛水すると有機物分解促進 |
生物圏-岩石圏-水圏-大気圏間炭素交換 → 炭素保管庫 reserver陸上生態系炭素循環大気中のCO2・水中のCO2 光合成┃呼吸 [ 植食植物 ] ↑呼吸 ↑呼吸 [光合成細菌] →[草食動物] ──→[肉食動物] ││ 摂食 │ 捕食 │ ↓└───→枯死 └→排出・死体←┘ 堆積・炭化─→ 堆積・炭化─┴─→[微生物] 石油・石炭CO2放出
腐敗菌による分解 ≈ 1.5 × 1011 C t/yr |
植物利用光エネルギー = 1.5 × 1020 kcal/yr メタン循環 (methane cycle)CH4発生 : 汚水 → 清流生息生物はO2不足で生息不可Ex. 生活廃水・排泄物等流入ドブ川(化学物質考えない) 生活排水 = ある細菌には栄養分(有機物)豊富高栄養分水流入 → 空気接触面(水表面)で有機物を空気中酸素で酸化しエネルギーにする従属栄養細菌増殖(好気性菌) → 溶存酸素(DO)減少 + 水に溶け込む酸素量減少 = 嫌気性条件下 (水表面近くで普通細菌が殖えると表面以下の水の中は嫌気性) → 嫌気性環境では好気性細菌は酸素不足で生存不可 嫌気性環境: 嫌気性(従属栄養)細菌が有機物を栄養分として利用し増殖開始嫌気性菌増殖 → 水環境は更にDO↓ → 嫌気性状態 → 通常細菌生存不可 |
|
農薬汚染 pesticide contamination: 農薬散布後に作物・土壌・水等に残留・蓄積し、生物や人間の健康に有害な環境をもたらすこと
(特に)難分解成分 → 自然生態系に影響 → 人体吸収 → 健康リスク 農薬は一部が大気中にドリフト(微粒子)拡散し土壌浸透後の揮発等で大気中に含まれ、大気中ダストにより世界中へ移動 (Peterle 1969)
南極大陸でpp'-DDTが0.04 ppb検出 水溶性低い農薬ほど底性沈殿物に早く吸収される。止水では水中で検出される農薬残留物は僅かだが、大部分が底性沈殿物となり、豪雨等で撹乱されると急速に水中に表れ漁業被害等として表れる 生態濃縮 (biomagnification)汚染物質が生態系中へ入り食物連鎖で高位消費者へ移る時に高率で濃縮生体内難分解性物質・放射性物質が、食物連鎖で選択的に濃縮 地表面や湖底表面に蓄積 → 生物に直接吸収され体内脂肪に残留 → 食物連鎖通し濃縮
Ex. 有機塩素系農業(DDT, BHC)、PCB、重金属化合物
陸上より多生物種が長い食物連鎖を作る水界で生態濃縮顕著 |
地球上で最もPCB汚染された人々 = 自然豊かなグリーンランド西方の島々
食糧の多くを魚、アザラシ、ホッキョクグマに依存
[リンゴ園 (10万ha)] [湖底泥 ] × 30 [底生端脚類]
図. ミシガン湖における流亡DDTの生態濃縮 (Hickey et al. 1966)。セグロカモメは、30 × 9 × 27 = 7290倍の濃縮となっている
[ 30t DDT/yr]─→[0.014 ppm]───→[ 0.41 ppm] [コオリガモ(胸筋)] ←───┬────────────┤ [ 6.33 ppm] × 15 ↓ × 9 ↓ × 14 [セグロカモメ ] [サケ幼魚] [マス ] [ 99.0 ppm ] [3.35 ppm] [5.6 ppm] [ 脳 20.8 ppm ] ←─┘ × 27 [ 体脂肪 2441 ppm ]
湿重当り(1g当たり) → エサとしての生物の汚染度を表す → 土壌・海底等中に蓄積された薬剤が次々濃縮され、人間を含む生物体内蓄積増える(Cox 1970) ポストハーベスト post-harvest: 農産物輸送・保存中の変質、虫害防止に収穫後用いる薬剤
殺虫剤、防カビ剤、防腐剤、変質防止剤など千種類以上 Def. 生物濃縮 bioconcentration or bioaccumulation: 生物が環境(Ex. 水、土壌)から直接(有害)物質取込み体内蓄積する現象 (≈ 生態濃縮) |
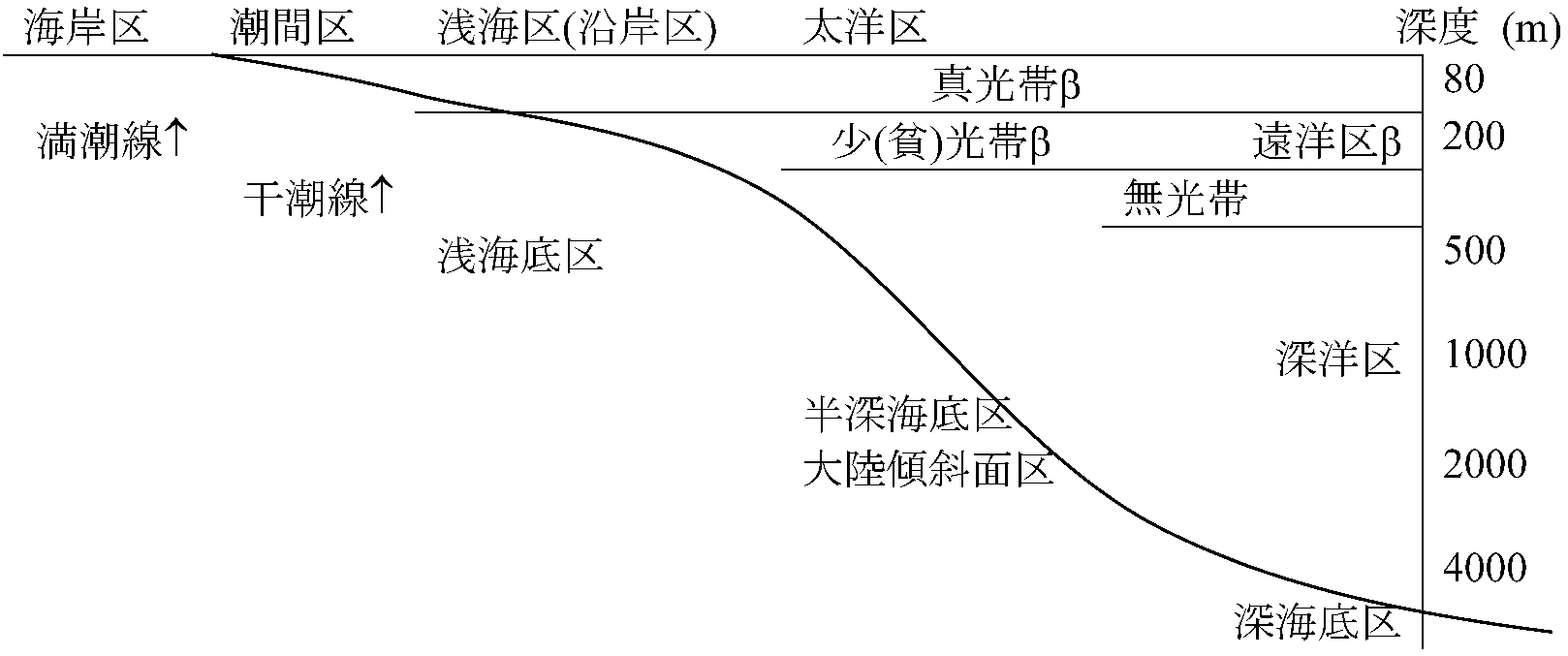 一次生産: 北極海の低生産力は植物プランクトン生産力差に加え、短増殖期間関与。南極海はbloom状態呈したり、北極海の1 gc/m²に比べ生産力高く、局部的差異目立つ。一次生産にphytoplanktonが大きな役割果たす 二次生産: 動物プランクトンzooplanktonは一次生産に付随し、周期変動もphytoplanktonに遅れ起こる。南極域ではzooplankton中で最も重要なものにオキアミ(ca 80 spp.)がある Ex. ヒゲクジラとオキアミの分布は概ね一致 Def. 成層 stratification: 水塊が密度の違いによって上下に分かれる現象 停滞期 = 成層の成立している時期
表水層(混合水層) epillimnion: 大気とガス交換 野外調査法
採泥器 sediment or bottom sampler: 湖底海底の堆積物・底生生物採取 Def. 透明度: 水中の光透過率・減衰率 - セッキー円板 Sacchi disk使用 Def. 透視度: 水中の清濁を知る指標 - 標識板 ランバート・ベーア則 (Lambert-Beer law)= ランバート則(光強度 ∝ 吸収層厚) + ベーア則(光強度 ∝ 濃度)log(I/I0) = -KD I: 光強度、I0: 直達光強度(D = 0)、K: 吸光係数(濃度)、D: 吸収層厚 D = 葉面積指数(leaf area index, LAI) ⇒ 植物群集での日射減衰 補償深度 compensation depth: 水深 ⇒ 有機物生産(光合成) = 消費(呼吸)
日補償深度: 夜間呼吸含めた1日の補償深度(通常はこれを意味) = 補償深度より浅い層 ↔ 無光層(栄養分解層、有機物分解層: 水深 ⇒ 有機物生産 < 消費補色適応説(Engelmann 1884)その深さに達する波長光を吸収する補助色素(フコキサンチン、フコエリトリン等)を持つものが生育に有利。海藻分布は到達光色と補色関係があり、紅藻・褐藻は短波長光を有効利用でき深所に生息可能。他に光量や酸素量等の要素が組合わさり、海藻垂直分布は決定される浅所: 緑藻類(Chl a, b, カロチン, キサントフィル) 例外: アサクサノリ(紅藻) = 浅い水面 深所: 褐藻類(Chl a, b, フコキサンチン)、紅藻類(Chl a, d, フィコエリトリン, フィコシアニン) Codium (ミル): シフォネイン、シフォキサンチン(キサントフィル色素)を持ち、深所にも生息可能 最高高潮面 --------------------------------------------------------------------大潮高潮面 ---------------------------- フノリ アサクサノリ --------------- 潮間帯 (小潮高潮面-小潮低潮面) ヒトエグサ ヒジキ ┏小潮高潮面 -------------------------------------------------------------------- ┃ アオノリ ┃ ウミウチワ アオサ ┃平均水面 ----------------------------------------------------------------------- ┃ スギノリ ソゾ オゴノリ ┃ ムカデノリ ┃ ツノマタ ミル ┗小潮低潮面 _________________________________________ 大潮低潮面 ホンダワラ アラメコンブ 海中林(= 藻場): 大型藻類繁茂する所 カジメ ワカメ トカサノリ テングサ 図. 藻類の垂直分布 |
沿岸帯 (littoral zone) ☛ 湖沼成帯構造: 殆どの沿岸群集で3帯発達↓ 潮上帯 supratidal zone (supralittoral zone) ↓ 真潮間帯 eulittoral zone 潮間帯 intertidal zone (tidal zone): 高潮線(大潮最高高潮線)と低潮線(大潮最低低潮線)に挟まれた海浜部 ↓ 亜潮間帯 sublittoral zone要因: 1, 潮汐原因説. 2, 物理化学的要因説(しぶき、塩分濃度勾配) タイドプール(潮溜り) tide pool (rock pool, 英): 潮間帯岩礁上水溜まる窪み 潮間帯だが常に海水に浸る(実質、潮下帯) - 独特な生態系構成 アマモ場(甘藻場, アジモ場): アマモ群生地 - 重要海産動物成育環境水生生物 (aquatic organism)生育型 → 水の動き(水流)が重要 (Haeckel 1891)プランクトン(浮遊生物) plankton: 遊泳能力欠くか極小 → 水流に運ばれる
Ex. クラゲ・プランクトン
植食性ネクトン(一次消費者) + 肉食性ネクトン(多次消費者)
Ex. 海藻・水草・フジツボ・ウニ・ナマコ 付着藻類 periphyton: 付着生物のうちで特に藻類のみを指す + セストン seston: 水中に浮遊する全ての固形物質(Kolkwitz 1912)
≈ 懸濁物質 suspended solids (SS)
(+ 海産種子植物(海草)種子)
非生セストン(生物死骸と分解産物、土砂・粘土等微粒子) ≡ トリプトン 水流帯多くの海藻は複数の帯にまたがり生育
遷移 (succession)群集作る比較的大きい空間形成後、その空間占める群集組成が時間と共に変化することEx. 珪藻類 → 成長速度速い藻類 + 付着動物 → 大型藻類 促進モデル facilitation model: 後の優占種は前の優占種により決まる耐性モデル tolerance model: 後の優占種は前の優占種と無関係 抑制モデル inhibition model: 後の優占種は前の優占種が消えるまで優占しない |
| 環境問題 environmental issues | |
|---|---|
海洋汚染河川からの汚濁物質流入、船舶からの油流出、廃棄物海洋投棄等が原因
PCB・水銀等の生態濃縮性物質による海洋汚染 → 魚介類への影響大 + 食物連鎖 → 人へ Def. 赤潮 red tide: (植物)プランクトン大量発生 (+ 水が変色)
本来は海域での異常発生のみを指す 密度: > 1000 cells/1 ml or 500 mg chlorophyll a/m3が目安 植物プランクトン phytoplankton
藍藻類 Cyanophyta: Trichodesmium, Anabaena, Microcystis 原生動物 Protozoa、有鞭毛虫 Mastigophora等 被害に関する説: 魚類等に大きな被害(漁業)
水塊の季節的循環(循環期か混合期) + 富栄養化が原因なことがある |
発生機構: 不明な点が多い a. 発生現地状況
Def. 青潮 blue tide (全く異なる2つの使い方)
1. 海洋で低(無)酸素水塊の湧昇現象 氷雪プランクトン: 氷雪上に成育する藻類 → 光合成色素で氷雪着色
高温で消失 (4°Cで多くが消失)
紅雪 (Chlamydomonas, Scotiella, Chodatella)、黄雪 (Scotiella)、緑雪(Ankistrodesmus)、褐雪(Mesotaenium)等 低酸素濃度海水が海面に上昇 → 青白い = 青潮 ⇒ 低酸素 + H2S(有毒)発生 → 生態系被害 Def. 軟泥 ooze: 湖沼・海洋底層に微粒子堆積し生じる泥 = 有機泥 + 赤色泥有機泥 orgnic mud: 生物遺骸起源 (= 骸泥 gyttja)
石灰質軟泥 calcareous ooze Ex. 有孔虫、翼足類 Def. 白化現象: サンゴが色あせ白っぽくなる現象 サンゴ: 体内の褐虫藻が光合成行う → サンゴ生息適温 = 25-29°C
海水温2°C↑ → 褐虫藻がサンゴから出る = 色抜ける → 褐虫藻戻らないとサンゴ死滅 |